
книги / Материаловедение.-1
.pdfМинистерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего образования «Пермский национальный исследовательский политехнический университет»
МАТЕРИАЛОВЕДЕНИЕ
Утверждено Редакционно-издательским советом университета
в качестве учебного пособия
Издательство Пермского национального исследовательского
политехнического университета
2017
УДК 620.22 М34
Авторы: Н.Н. Митрохович, С.С. Югай, О.В. Силина, Т.Н. Некрасова, М.Г. Закирова, Д.О. Панов
Рецензенты:
д-р техн. наук, профессор Ю.Н. Симонов (Пермский национальный исследовательский политехнический университет);
чл.-корр. РАЕН, д-р техн. наук, профессор Л.В. Спивак (Пермский государственный национальный исследовательский университет)
Материаловедение : учеб. пособие / Н.Н. Митрохович М34 [и др.]. – Пермь : Изд-во Перм. нац. исслед. политехн.
ун-та, 2017. – 195 с.
ISBN 978-5-398-01765-6
Кратко изложены основные теоретические разделы курса «Материаловедение». Представлена программа курса. Приведены варианты заданий для выполнения контрольной работы.
Предназначено для студентов вузов очной и заочной формы обучения металлургических и машиностроительных специальностей.
УДК 620.22
ISBN 978-5-398-01765-6 |
© ПНИПУ, 2017 |
ОГЛАВЛЕНИЕ |
|
Тема1. Атомно-кристаллическоестроениеметаллов.............................. |
6 |
Тема2. Деформация, разрушениеимеханические |
|
свойстваметаллов.......................................................................................... |
12 |
2.1. Упругая и пластическая деформация. |
|
Пути повышения прочности................................................. |
12 |
2.2. Наклеп и рекристаллизация.................................................. |
15 |
2.3. Понятиеохолоднойигорячейдеформации.......................... |
17 |
2.4. Механические свойства металлов........................................ |
18 |
Тема3. Основытеориисплавов. Диаграммысостояния........................ |
21 |
3.1. Основные виды диаграмм состояния................................... |
21 |
3.2. Практическое значение диаграмм состояния..................... |
24 |
Тема4. Диаграммасостояния железо – цементит.................................. |
28 |
Тема5. Превращения всталях принагреве иохлаждении................... |
33 |
Тема6. Основные видытермическойобработкисталей........................ |
37 |
Тема7. Основылегирования сталей........................................................... |
44 |
7.1. Общие вопросы теории легирования сталей....................... |
44 |
7.2. Особенности термической обработки |
|
легированных сталей................................................................. |
49 |
Тема8. Маркировкасталейв России......................................................... |
51 |
8.1. Классификация сталей........................................................... |
51 |
8.2. Маркировка углеродистых сталей........................................ |
52 |
8.3. Маркировка легированных сталей....................................... |
54 |
Тема9. Маркировкасталейпоевронормам.............................................. |
60 |
9.1. Маркировка сталей по назначению и механическим |
|
или физическим свойствам................................................... |
60 |
9.2. Маркировка сталей по химическому составу.................... |
65 |
Тема10. Конструкционныестали............................................................... |
68 |
Тема11. Инструментальныестали............................................................. |
77 |
3
Тема12. Стали соспециальными свойствами. |
|
Коррозионно-стойкиестали......................................................................... |
82 |
12.1. Коррозия металлов и ее виды............................................. |
82 |
12.2. Коррозионно-стойкие стали................................................ |
83 |
12.2.1. Стали ферритного класса ............................................ |
85 |
12.2.2. Стали мартенситного класса....................................... |
88 |
12.2.3. Стали мартенсито-ферритного класса ....................... |
89 |
12.2.4. Хромоникелевые нержавеющие стали....................... |
90 |
12.3. Жаростойкие стали............................................................... |
92 |
12.4. Жаропрочные стали и сплавы............................................. |
92 |
Тема13. Методыповерхностного упрочнениястальныхдеталей....... |
96 |
13.1. Поверхностная закалка стали.............................................. |
96 |
13.2. Химико-термическая обработка металлов........................ |
98 |
13.2.1. Общие закономерности ХТО...................................... |
98 |
13.2.2. Цементация................................................................... |
99 |
13.2.3. Азотирование.............................................................. |
100 |
13.2.4. Совместное насыщение углеродом и азотом............ |
102 |
13.2.5. Борирование................................................................ |
103 |
13.2.6. Диффузионная металлизация.................................... |
104 |
Тема14. Цветныеметаллыи сплавы........................................................ |
106 |
14.1. Алюминий и сплавы на его основе .................................. |
106 |
14.2. Медь и сплавы на ее основе.............................................. |
110 |
14.3. Титан и сплавы на его основе........................................... |
112 |
14.4. Никель и сплавы на его основе......................................... |
114 |
Тема15. Неметаллическиематериалы..................................................... |
117 |
15.1. Органические неметаллические материалы.................... |
117 |
15.1.1. Полимеры.................................................................... |
118 |
15.1.2. Резиновые материалы................................................ |
121 |
15.1.3. Лесоматериалы........................................................... |
122 |
15.2. Неорганические неметаллические материалы............... |
124 |
15.2.1. Неорганические стекла.............................................. |
124 |
15.2.2. Ситаллы (стеклокерамика) ........................................ |
126 |
15.2.3. Техническая керамика ............................................... |
127 |
15.2.4. Каменные материалы ................................................ |
127 |
15.2.5. Неорганические вяжущие вещества ........................ |
129 |
4
Тема16. Композиционные материалы .................................................... |
130 |
16.1. Композиционные материалы на основе |
|
металлической матрицы ................................................... |
130 |
16.2. Композиционные материалы на основе |
|
полимерной матрицы ........................................................ |
133 |
Задания для контрольной работы ............................................................. |
135 |
Программакурса«Материаловедение» .................................................. |
190 |
Список литературы ..................................................................................... |
194 |
5
ТЕМА 1. АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
Все металлы и металлические сплавы в обычных условиях являются кристаллическими телами, в которых атомы (ионы) расположены в определенном порядке. Кристаллическая решетка представляет собой воображаемую пространственную сетку; атомы металла располагаются в узлах сетки. Наименьший объем, дающий представление об атомно-кристаллической струк-
туре в целом, называется элементарной кристаллической ячейкой. Большинство металлов образуют одну из следующих решеток: кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную плотноупакованную (ГПУ). Эти решетки отличаются высокой симметрией
ибольшой плотностью упаковки атомов (в 1 см3 содержится более 1022 атомов). Поскольку именно атомы являются мельчайшими составляющими любого технического материала, то многие характеристики и свойства атомов приобретают особое значение. Так, атомная масса определяет плотность и теплоемкость твердых тел, а структура электронных оболочек влияет на характер межатомного взаимодействия и прочность межатомных связей.
Атомы металлов содержат на внешнем энергетическом уровне небольшое количество электронов, поэтому они, имея слабую связь с ядром, способны легко отделяться от атомов
инаходиться в относительно свободном состоянии. При взаимодействии атомов металлов происходит обобществление валентных электронов в объеме всего кристалла. Подвижность множества валентных электронов («электронного газа», «электронного облака») определяет такие свойства металлов, как высокая электропроводность и теплопроводность, блеск, непрозрачность. Чем больше плотность «электронного газа», тем сильнее межатомная связь. Для большинства случаев (табл. 1) с увеличением
6
энергии связи Eсв растут температура плавления Tпл, модуль упругости Еупр, энергия активации самодиффузии Qдиф; коэффициент линейного расширения α, наоборот, уменьшается. Исключения: аномально завышен модуль упругости у бериллия, что позволяет использовать его сплавы как материалы повышенной жесткости; титан и цирконий имеют заниженные значения модуля упругости и энергии активации самодиффузии. Последнее объясняет их пониженную жаропрочность.
Ненаправленность металлической связи, когда каждый атом стремится притянуть к себе как можно больше соседних атомов, определяет большую компактность кристаллических структур металлов. В наиболее плотноупакованных кристаллах (ГПУ и ГЦК) каждый атом может иметь 12 соседей (координационное число К12). В решетке объемноцентрированного куба для каждого атома число ближайших равноудаленных элементарных частиц равно 8 (К8). Благодаря образованию плотноупакованных структур металлические кристаллы более пластичны и менее тверды, чем кристаллы с ковалентным типом связи.
Таблица 1
Энергия межатомной связи и свойства металлов
Металл |
Есв, |
Tпл, |
α 106, °С–1 |
Еупр, |
Qдиф, |
ρ, г/см3 |
кДж/гатом |
°С |
(25–100 °С) |
ГПа |
кДж/гатом |
(25 °С) |
|
Магний |
151 |
650 |
26 |
45 |
134 |
1,7 |
Алюминий |
232 |
660 |
24 |
71 |
142 |
2,7 |
Медь |
340 |
1083 |
16 |
121 |
197 |
8,9 |
Бериллий |
– |
1284 |
12 |
310 |
160 |
1,8 |
Железо |
396 |
1539 |
12 |
214 |
250 |
7,8 |
Титан |
419 |
1665 |
9,9 |
112 |
122 |
4,5 |
Цирконий |
460 |
1852 |
9,6 |
70 |
92 |
6,5 |
Хром |
– |
1875 |
6,2 |
280 |
310 |
7,1 |
Ванадий |
– |
1919 |
8,7 |
135 |
398 |
6,1 |
Ниобий |
– |
2468 |
7,2 |
124 |
398 |
8,6 |
Молибден |
670 |
2625 |
5,1 |
334 |
424 |
10,2 |
Тантал |
– |
3000 |
6,5 |
185 |
460 |
16,6 |
Вольфрам |
880 |
3410 |
4,4 |
420 |
500 |
19,3 |
7
Около тридцати металлов (Fe, Ti, Sn, Co и др.) обладают температурным полиморфизмом. Полиморфизм технических материалов имеет крайне важное значение для их обработки и эксплуатации. Например, термообработка сталей основана на стабилизации ГЦК-структуры железа при высокой температуре с переходом ее в ОЦК-структуру во время охлаждения.
Пример. Описать аллотропические превращения в железе. Построить кривую охлаждения для железа в интервале температур
1600–20 °С.
Решение. Аллотропией, или полиморфизмом, называют способность металла в твердом состоянии иметь различные кристаллические формы. Процесс перехода из одной кристаллической формы в другую сопровождается поглощением тепла (при нагреве) или выделением тепла (при охлаждении), поэтому в чистых металлах такие превращения происходят при постоянной температуре. Например, железо в интервале температур 911–1392 °С имеет гранецентрированную кубическую решетку ГЦК – γ-железо; при температурах до 911 °С и от 1392 до 1539 °С железо имеет решетку ОЦК – α-железо:
911 1392
α-Fe → γ-Fe → α-Fe (δ-Fe).
Аллотропические формы железа, как и других металлов, обозначают буквами греческого алфавита. Кривая охлаждения для железа приведена на рис. 1.
Следует отметить, что все кристаллические тела не обладают совершенной кристаллической структурой, а содержат различного рода «дефекты» – несовершенства структуры
(вакансии, межузельные атомы, дислокации, границы зерен), возникающие в результате смещения или удаления атомов со своих мест в решетке. Если бы все реальные материалы имели совершенную структуру, они не обладали бы пластичностью и не поддавались обработке, необходимой для изготовления деталей. Термообработка и улучшение свойств сталей основаны не только на изменении структуры, но и на сопутствующих
8
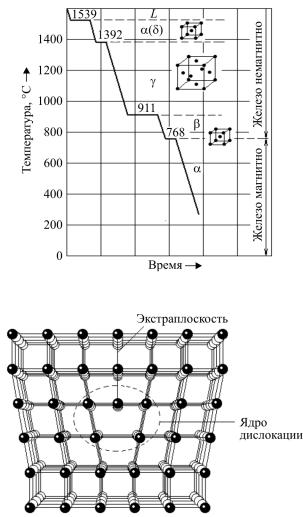
им изменениях несовершенств. Наиболее важным видом несовершенств, определяющим механические свойства металлов, являются дислокации (рис. 2).
Рис. 1. Аллотропические превращения в железе
Рис. 2. Дислокация в кристаллической решетке
9
Так, любая пластическая деформация является результатом движения и одновременного генерирования дислокаций. У отожженных металлов плотность дислокаций, т.е. суммарная длина всех линий дислокаций в единице объема, равна 106–107 см–2. Дислокации, как и другие несовершенства кристаллического строения, появляются в металлах при кристаллизации.
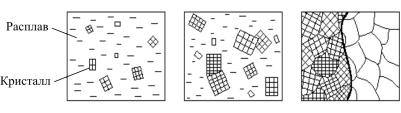
Кристаллизацией называется переход металла из жидкого состояния в твердое с образованием кристаллической структуры. Затвердевание происходит путем образования центров кристаллизации (зародышей) и их роста. Пока кристаллы растут свободно, они имеют правильную геометрическую форму. Однако при столкновении растущих кристаллов их правильная форма нарушается, так как прекращается рост отдельных граней, и образу-
ются кристаллиты, или зерна (рис. 3).
Рис. 3. Схема процесса кристаллизации (показана кристаллографическая ориентация зерен)
Форма и размер зерен зависят от условий их роста: скорости и направления отвода тепла, температуры жидкого металла и др. Типичная структура слитка металла состоит из трех зон: мелких равноосных кристаллов на поверхности слитка, зоны столбчатых кристаллов, расположенных нормально к стенкам формы, и равноосных кристаллов больших размеров в середине слитка. Применяя различные технологические приемы, можно изменять количественное соотношение зон.
10
