
7467
.pdfМИНОБРНАУКИ РОССИИ Федеральное государственное бюджетное образовательное учреждение высшего
образования «Нижегородский государственный архитектурно-строительный университет»
Д.Б. Жесткова
ЛАБОРАТОРНЫЕ РАБОТЫ ПО ФИЗИОЛОГИИ РАСТЕНИЙ
Учебно-методическое пособие по выполнению лабораторных работ по дисциплине «Физиология растений»
для обучающихся по направлению подготовки 35.03.10 Ландшафтная архитектура
Нижний Новгород
2022
1
МИНОБРНАУКИ РОССИИ Федеральное государственное бюджетное образовательное учреждение высшего
образования «Нижегородский государственный архитектурно-строительный университет»
Д.Б. Жесткова
ЛАБОРАТОРНЫЕ РАБОТЫ ПО ФИЗИОЛОГИИ РАСТЕНИЙ
Учебно-методическое пособие по выполнению лабораторных работ по дисциплине «Физиология растений»
для обучающихся по направлению подготовки 35.03.10 Ландшафтная архитектура
Нижний Новгород ННГАСУ
2022
2
УДК 596(075.8)
Жесткова Д. Б. Лабораторные работы по физиологии растений: учебно-методическое пособие / Д.Б. Жесткова; Нижегородский государственный архитектурностроительный университет. – Нижний Новгород : ННГАСУ, 2022. – 33 с; ил. - Текст : электронный.
В учебно-методическом пособии дается подробное описание хода выполнения лабораторных работ по физиологии растений при изучении дисциплины «Физиология растений», рассматриваются теоретические вопросы, приводятся схемы, рисунки, дается перечень материалов и оборудования для каждого занятия.
Предназначено для обучающихся в ННГАСУ по направлению подготовки 35.03.10 Ландшафтная архитектура.
©О. П. Лаврова, Д.Б. Жесткова, 2022
©ННГАСУ, 2022.
3
СОДЕРЖАНИЕ
1. Занятие 1………………………………………………………… |
4 |
2. Занятие 2 ………..………………………………………………. |
10 |
3. Занятие 3 ………………………………………………………... |
14 |
4. Занятие 4 …………………………………………………..……. |
17 |
5. Занятие 5 ………………………………………………………... |
19 |
6. Занятие 6 ………………………………………………………... |
23 |
7. Занятие 7 ………………………………………………………... |
27 |
8. Занятие 8 ………………………………………………………... |
33 |
Литература ………………………………………………………… |
34 |
4
ЗАНЯТИЕ 1.
Тема: Физиология растительной клетки.
Работа № 1. Плазмолиз и деплазмолиз. Формы плазмолиза.
Цель работы: пронаблюдать плазмолиз и деплазмолиз в клетках лука репчатого. Отметить формы плазмолиза клеток.
Оборудование: микроскопы, предметные и покровные стекла,
полоски фильтровальной бумаги, пинцеты, скальпели, пипетки, кюветы с водой.
Материалы и реактивы: луковица лука репчатого красного цвета,
раствор поваренной соли (NaCl).
В растительной клетке важнейшую роль выполняет полупроницаемая мембрана, которая состоит из плазмалеммы, тонопласта и расположенной между ними цитоплазмы. Избирательная проницаемость
(полупроницаемость) плазмалеммы и тонопласта заключается в том, что они легко пропускают воду и с трудом пропускают или не пропускают растворенные в ней вещества. Поступление воды в клетку связано с вакуолью. В ней содержатся ионы, сахара, органические кислоты,
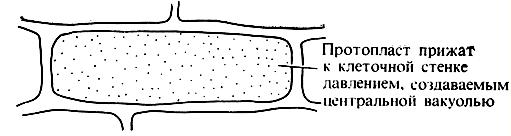
формирующие раствор, концентрация которого выше, чем в свободном пространстве клеточной стенки (рис. 1).
Рис. 1. Клетка чешуйки лука репчатого в нормальном состоянии.
5
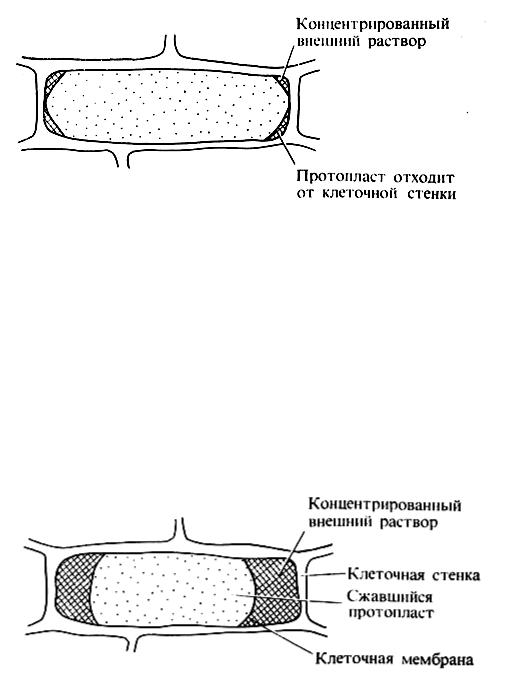
Растительная клетка функционирует как осмотическая система, что подтверждает плазмолиз. Плазмолиз – это процесс отделения протопласта от клеточной стенки (рис. 2). Он происходит при погружении клетки в раствор, концентрация которого выше, чем концентрация клеточного сока.
Рис. 2. Клетка чешуйки лука репчатого в начале плазмолиза.
В таких условиях молекулы воды из клетки выходят значительно быстрее, чем наблюдается их поступление в клетку, что приводит к снижению содержания воды в клетке (в первую очередь в вакуоли) и
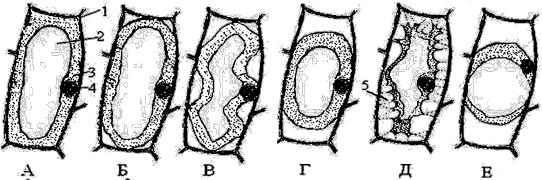
отделению протопласта от клеточной стенки (рис. 3). Выход воды из клетки будет продолжаться до тех пор, пока концентрации клеточного сока и внешнего раствора не сравняются.
Рис. 3. Клетка чешуйки лука репчатого в состоянии выпуклого плазмолиза.
6
По мере развития в клетке плазмолиза форма протопласта меняется:
сначала протопласт отделяется от клеточной стенки лишь в уголках
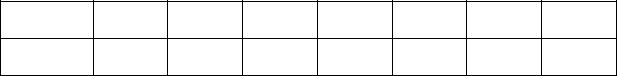
(уголковый плазмолиз), затем у него появляются многочисленные вогнутые поверхности (вогнутый плазмолиз) и, наконец, протопласт полностью отрывается от клеточной стенки и под действием сил поверхностного натяжения принимает округлую форму (выпуклый плазмолиз). Если вогнутый плазмолиз выражен чрезмерно, то говорят о судорожном плазмолизе (рис. 4).
Рис. 4. А – Клетка чешуйки лука репчатого в нормальном состоянии: 1 – клеточная оболочка, 2 – вакуоль, 3 – цитоплазма, 4 – ядро; Б – уголковый плазмолиз клеток чешуйки лука; В, Д – судорожный плазмолиз; Г – вогнутый плазмолиз; Е – выпуклый плазмолиз.
Пространство между клеточной стенкой и плазмалеммой,
образующееся во время плазмолиза, заполняет раствор плазмолитика – вещества, вызывающего плазмолиз. В качестве плазмолитиков могут выступать неядовитые вещества, например, сахара (сахароза, глюкоза,
ксилоза и др.), некоторые соли (NaCl, KCl, KNO3). К плазмолизу способны только живые клетки, у которых плазмалемма и тонопласт обладают свойством избирательной проницаемости.
Плазмолиз обратим. Процесс, обратный плазмолизу, называется деплазмолизом. Он развивается при погружении плазмолизированной клетки в чистую воду или раствор, концентрация которого ниже, чем концентрация клеточного сока. Деплазмолиз протекает быстрее, чем
7
плазмолиз, и не имеет промежуточных стадий. По мере увеличения содержания воды в клетке объем вакуоли возрастает, клеточный сок давит на цитоплазму и прижимает ее к клеточной стенке. Под влиянием внутреннего давления клеточная стенка незначительно растягивается, а
сама клетка переходит в напряженное состояние – тургор.
Ход работы: Берут луковицу лука репчатого красного цвета и отделяют от нее несколько сочных чешуек (видоизмененных листьев).
Необходимо сделать тонкий срез с нижней стороны чешуйки или пинцетом снимают тонкий слой кожицы. Срез помещают на предметное стекло в каплю воды и накрывают покровным стеклышком. Помещают полученный временный препарат под малое увеличение микроскопа. Под микроскопом должны наблюдать равномерно окрашенные клетки чешуйки лука, богатые антоцианом.
К препарату с одной стороны покровного стекла начинают по капле добавлять раствор хлористого натрия (NaCl), а с другой стороны – фильтровальной бумагой оттягивать лишнюю влагу.
Через короткое время наблюдают, что внутреннее содержимое клеток, протопласт, начинает отслаиваться от уголков клеточной стенки, а
затем и от всей поверхности. Так происходит плазмолиз клеток, или их защитная реакция на воздействие раствора соли.
Если, напротив, начинают добавлять воду к препарату,
содержимое клеток примет изначальную форму. Это деплазмолиз клеток.
По окончании работы выполняют рисунки в тетради и делают выводы о наблюдаемой степени плазмолиза клеток лука репчатого.
8
Работа № 2. Определение осмотического давления клеточного сока плазмолитическим методом.
Цель работы: определить осмотическое давление клеточного сока в клетках лука репчатого плазмолитическим методом.
Оборудование: микроскопы, предметные и покровные стекла, чашки Петри, полоски фильтровальной бумаги, пинцеты, скальпели, пипетки,
кюветы с водой.
Материалы и реактивы: луковица лука репчатого красного цвета,
раствор поваренной соли (NaCl).
Ход работы: В разные чашки Петри наливают растворы NaCl
различной концентрации. Одновременно на каждую чашку Петри делают не менее четырех свежих срезов лука репчатого красного цвета. Засекают
30 минут и помещают срезы в растворы соли.
По истечении времени рассматривают срезы чешуек лука под микроскопом. Замечают концентрацию поваренной соли, при которой наблюдается тот или иной вид плазмолиза клеток лука. Все данные заносят в таблицу.
Таблица.
Степени плазмолиза клеток лука репчатого при разных концентрациях раствора NaCl
C, NaCl, |
1,0 |
0,8 |
0,6 |
0,4 |
0,2 |
0,1 |
H2O |
моль
Степень
плазмолиза
Обязательно отмечают концентрацию соли, при которой плазмолиз
клеток прекращается.
9
Для определения осмотического давления в клетках лука,
используют уравнение Вант-Гоффа:
P=R*T*C*I, где
R – универсальная газовая постоянная, равна 0,0821 атм/К*моль,
T – абсолютная температура в К,
C – концентрация раствора соли NaCl,
I – изотонический коэффициент, равен 1,75.
Выполняют расчет осмотического давления в клетках и делают вывод о наблюдаемой степени плазмолиза клеток лука репчатого.
Работа № 3. Осмотический выход воды из клеток, подвергающихся плазмолизу.
Цель работы: пронаблюдать осмотический выход воды из клеток паренхимы моркови в результате плазмолиза.
Оборудование: стеклянные стаканчики, чашки Петри, пинцеты,
скальпели, пипетки, деревянные палочки, кюветы с водой.
Материалы и реактивы: корнеплод моркови, раствор NaCl.
Ход работы: Берут 2 брусочка ткани паренхимы корнеплода моркови и помещают один в сосуд с водой, второй – в сосуд с раствором поваренной соли (NaCl). Очень скоро наблюдают, что в сосуде с раствором соли вода начинает выходить из клеток паренхимы в виде тонких струек, отходящих от поверхности кусочка моркови. В сосуде с водой ничего не происходит.
После наблюдения зарисовывают опыт и делают вывод об условиях плазмолиза клеток паренхимы корнеплода моркови.
