
4 курс / Дерматовенерология / ТРЕГАЛОЗА_ОСОБЕННОСТИ_ХИМИЧЕСКОГО_СТРОЕНИЯ
.pdf
МИКРОБИОЛОГИЯ, 2014, том 83, № 3, с. 271–283
ОБЗОР
УДК 577.114:579.22
ТРЕГАЛОЗА: ОСОБЕННОСТИ ХИМИЧЕСКОГО СТРОЕНИЯ, БИОЛОГИЧЕСКИЕ ФУНКЦИИ И ПРАКТИЧЕСКОЕ ЗНАЧЕНИЕ
© 2014 г. Е. П. Феофилова*, 1, А. И. Усов**, И. С. Мысякина*, Г. А. Кочкина***
*Институт микробиологии им. С.Н. Виноградского Российской академии наук, Москва **Институт органической химии им. Н.Д. Зелинского Российской академии наук, Москва
***Институт биохимии и физиологии микроорганизмов им. Г.К. Скрябина Российской академии наук, Пущино, Московская обл.
Поступила в редакцию 23.04.2013 г.
Обзор посвящен современным представлениям о химическом строении и свойствах трегалозы, распространении и биологических функциях у растений, грибов и прокариот, ее практическом использовании, главным образом, в медицине и биотехнологии. Отдельный раздел посвящен зна$ чению трегалозы и других протекторных полиолов при стреccе у грибов.
Ключевые слова: трегалоза, протекторные углеводы, микроорганизмы, мицелиальные грибы, бактерии.
DOI: 10.7868/S0026365614020074
ВВЕДЕНИЕ
Трегалоза была обнаружена в мицелии гриба р. Claviceps (спорыньи), паразитирующего на ржи, еще в 1832 г. [1]. Французский химик Марсе$ лен Бертло (Marcellin Berthelot) впервые получил этот дисахарид в достаточном количестве в виде сладкого вещества из гнезд и коконов насекомого
Larinus maculatus и L. nidificans. Отсюда, вероятно, и произошло название “трегалоза” – коконы жу$ ка называли “Trehala manna” [2, 3], хотя суще$ ствует еще одно название этого дисахарида – ми$ коза [4]. Оказалось, что трегалоза широко распро$ странена в природе и встречается в самых разнообразных организмах, от бактерий до беспо$ звоночных. Наибольшее количество трегалозы сосредоточено в спорах мицелиальных грибов и в дрожжах от 16 до 30% [5, 6]. Наличие этого саха$ ра у млекопитающих долгое время вызывало со$ мнения, хотя у некоторых людей еще в 1965 г. была обнаружена активная трегалаза – фермент, разла$ гающий в кишечнике трегалозу на две молекулы глюкозы [7] и являющийся маркером поврежде$ ния почечных канальцев [8]. Был обнаружен также специальный ген, участвующий в синтезе трегало$ зы, который идентифицирован у многих организ$ мов, имеющих очень низкий, трудно идентифици$ руемый уровень трегалозы. Эти данные позволяют предположить, что трегалоза является универсаль$ ным соединением, свойственным всему живому.
1Автор для корреспонденции (e$mail: feofilov@inmi.host.ru, biolog100@bk.ru).
К середине прошлого столетия был выполнен химический синтез трегалозы и накоплены об$ ширные сведения о метаболизме и природных ис$ точниках дисахарида [9, 10]. Длительное время трегалозу рассматривали как своеобразный энер$ гетический резерв, пока не появились сведения о сигнальных функциях и защитной роли дисаха$ рида в отношении белков и мембран при стрессо$ вых ситуациях, таких как дегидратация и тепловой шок. Эти данные привели к появлению множества работ, посвященных изучению специфических физико$химических свойств трегалозы и ее роли в живых системах. Количество работ, посвященных трегалозе, измеряется тысячами (например, к на$ чалу 2000 г. выполнено более 4600 исследований, где упоминается этот дисахарид [3]), а наиболее важные результаты отражены в ряде обзоров [2, 11–13 и другие]. Но только относительно недавно было осмыслено основное значение трегалозы: молекула этого сахара поддерживает и сохраняет (консервирует) в состоянии покоя жизнь при не$ благоприятных условиях существования (что, ве$ роятно, можно отнести к любому живому суще$ ству). Возможно, эту мысль можно выразить в бо$ лее определенной форме – трегалозе мы обязаны тем, что, несмотря на все “усилия” цивилизации, природа еще сохраняется на нашей планете. Обос$ нование этой идеи на примере ряда царств живой природы стало основной целью при написании на$ стоящего обзора, в котором также показано, как теоретические положения, касающиеся протек$ торной роли трегалозы, способствуют развитию исследований, направленных на практическое
271 |
2* |

272 ФЕОФИЛОВА и др.
CH2OH |
зико$химические свойства трегалозы подробно |
||||
HO |
O |
описаны в обзоре Отаке и Ванга [18]. Для препа$ |
|||
|
|
|
ративного получения сравнительно небольших |
||
HO |
|
|
|
||
|
|
|
количеств трегалозы предложена экстракция из |
||
HO O |
|||||
HO |
|
|
биомассы пекарских дрожжей [19]. |
||
|
|||||
HO |
|
|
|
Кроме свободной трегалозы, в природе встре$ |
|
|
|
|
|||
HO |
O |
чается несколько типов ее производных, среди |
|||
CH2OH |
которых можно назвать трегалозо$6$фосфат, про$ |
||||
Рис. 1. Строение молекулы трегалозы. |
межуточный продукт ее биосинтеза из уридинди$ |
||||
фосфатглюкозы и глюкозо$6$фосфата [8, 10]. Из$ |
|||||
|
|
|
|
вестны также продукты гликозилирования моле$ |
|
применение трегалозы, в частности, в медицине. |
кулы трегалозы, напоминающие аналогичные |
||||
производные сахарозы (раффинозу, стахиозу и |
|||||
На примере царства Mycota впервые представлены |
|||||
др.). Так, из микобактерий были выделены тет$ |
|||||
данные о взаимодействии |
трегалозы с другими |
||||
расахариды α$Glc$(1 → 4)$α$Glc$(1 ↔ 1)$α$Glc$ |
|||||
протекторыми соединениями (полиолами). |
|||||
(6 ← 1)$α$Gal, α$Gal$(1 → 6)$α$Gal$(1 → 6)$α$ |
|||||
|
|
|
|
||
|
|
|
|
Glc$(1 ↔ 1)$α$Glc и β$Glc$(1 → 6)$β$Glc$(1 → |
|
ХИМИЧЕСКОЕ СТРОЕНИЕ И СВОЙСТВА |
→ 6)$α$Glc$(1 ↔ 1)$α$Glc и трисахариды α$Glc$ |
||||
(1 → 4)$α$Glc$(1 ↔ 1)$α$Glc и β$Glc$(1 → 6)$α$ |
|||||
ТРЕГАЛОЗЫ И ЕЕ ПРОИЗВОДНЫХ |
|||||
Glc$(1 ↔ 1)$α$Glc [20]. Присутствие некоторых |
|||||
Молекула трегалозы построена из двух моле$ |
|||||
из этих олигосахаридов было отмечено также в |
|||||
кул D$глюкозы (рис. 1). Подобно сахарозе, еще |
|||||
других бактериях, насекомых и грибах. |
|||||
более распространенному дисахариду, трегалоза |
|||||
Необычными производными трегалозы явля$ |
|||||
не обладает восстанавливающими свойствами, по$ |
|||||
скольку у нее блокированы гликозидные группы |
ются гликолипиды, в которых остаток трегалозы |
||||
обоих остатков глюкозы. Исходя из того, что моно$ |
составляет полярную часть молекулы [21]. Такие |
||||
сахариды могут иметь α$ или β$конфигурацию и |
гликолипиды были обнаружены впервые в тубер$ |
||||
находиться в пиранозной или фуранозной форме, |
кулезных бактериях в качестве материала (они |
||||
теоретически возможны десять дисахаридов, со$ |
получили название “корд$фактора”), который |
||||
держащих связи 1 ↔ 1 между остатками D$глюко$ |
является фактором патогенности. В 1956 г. было |
||||
зы. Природный дисахарид построен из двух одина$ |
установлено, что корд$фактор представляет со$ |
||||
ковых остатков α$D$глюкопиранозы, его полное |
бой 6,6'$димиколат трегалозы. Строение миколо$ |
||||
название – α$D$глюкопиранозил$α$D$глюкопи$ |
вых кислот было затем предметом многочисленных |
||||
ранозид – для краткости обычно заменяют терми$ |
исследований. Стало известно, что это кислоты |
||||
ном α,α$трегалоза, или просто трегалоза. Изомер$ |
С60–С90 с разветвленной углеродной цепью и, по |
||||
ные α,β$трегалоза и β,β$трегалоза, отличающиеся |
крайней мере, двумя хиральными центрами в α$ и |
||||
только конфигурациями гликозидных центров, по$ |
β$положении к карбоксилу, имеющими R$конфи$ |
||||
лучены синтетически, а соответствующие дисаха$ |
гурацию [22]. В молекулах миколовых кислот раз$ |
||||
риды, содержащие фуранозные формы глюкозы, |
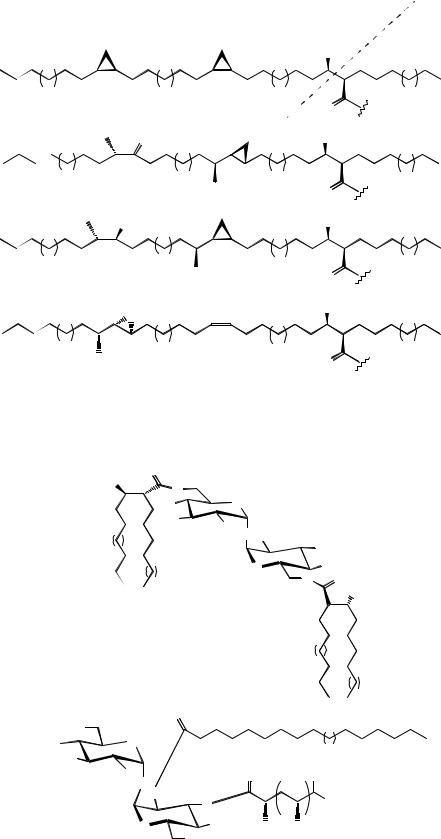
личают α$ветви и меромиколатные ветви (рис. 2). В |
||||
по$видимому, не известны. Установление строения |
гликолипидах, выделяемых из разных видов или |
||||
трегалозы классическими методами химии углево$ |
штаммов микобактерий, α$ветви миколовых кис$ |
||||
дов подробно описано в обзоре Берча [9]. |
лот различаются только длиной, тогда как меро$ |
||||
Благодаря хорошей растворимости в водно$ |
миколатные участки более вариабельны и могут |
||||
различаться функциональным составом. Чаще |
|||||
этанольных смесях трегалозу можно легко из$ |
|||||
всего эти участки содержат цис$циклопропано$ |
|||||
влечь из биологического материала экстракцией |
|||||
вые звенья, но встречаются и оксигенированные |
|||||
70–80%$ным этанолом при нагревании. Дисаха$ |
|||||
миколаты, содержащие метокси$, кето$ и эпокси$ |
|||||
рид кристаллизуется из водного этанола в виде |
|||||
группы [21] (рис. 2). |
|||||
дигидрата, т. пл. 96–97°С, [α]D +177–182, и может |
|||||
|
|||||
быть идентифицирован |
в виде октаацетата, |
Сходные с корд$фактором 6,6'$диацилпроиз$ |
|||
т. пл. 97–98°С, [α]D +163. Для количественного |
водные трегалозы были выделены из коринебак$ |
||||
микроопределения трегалозы применяют высо$ |
терий [23]. Входящие в их состав кориномиколо$ |
||||
коэффективную жидкостную хроматографию с |
вые кислоты имеют несколько более простое |
||||
внутренним стандартом [14] или действие высо$ |
строение по сравнению с миколовыми кислота$ |
||||
коспецифичного фермента трегалазы в комбина$ |
ми, хотя также содержат два хиральных центра, |
||||
ции с оксидазой D$глюкозы [15]. Трегалоза имеет |
имеющих R$конфигурацию (рис. 3) [22]. Чаще |
||||
характеристические спектры 1Н$ и 13С$ЯМР, ко$ |
всего в этих гликолипидах находят С32$кориноми$ |
||||
торые также можно эффективно использовать |
коловую кислоту, хотя встречаются также кислоты |
||||
для ее обнаружения и количественного определе$ |
с более короткими цепями (С24 С30) и их дегидро$ |
||||
ния в биологических объектах [16, 17]. Другие фи$ |
производные. Еще более простые кислоты обнару$ |
||||
МИКРОБИОЛОГИЯ том 83 № 3 2014
ТРЕГАЛОЗА: ОСОБЕННОСТИ ХИМИЧЕСКОГО СТРОЕНИЯ |
273 |
|||
|
|
меромиколатная ветвь |
альфа$ветвь |
|
|
|
OH |
|
|
x |
y |
z |
n |
|
|
|
O |
|
|
|
O |
OH |
|
|
x |
y |
z |
n |
|
|
|
O |
|
|
|
OMe |
OH |
|
|
x |
y |
z |
n |
|
x |
y |
O |
|
|
|
|
|
||
|
|
|
|
|
|
O |
OH |
|
|
|
|
|
|
|
x |
y |
z |
n |
|
O
Рис. 2. Остатки миколовых кислот в составе корд$фактора (x, y, z – общая длина цепи С60–С90, n = 13–19) [21].
|
O |
|
|
|
|
HO |
|
|
|
|
O |
|
O |
|
|
HO |
|
|
|
|
HO |
HO |
|
|
|
|
O OH |
|
|
|
10 |
|
|
|
|
|
|
OH |
|
|
|
|
O |
OH |
|
9 |
|
|
O O |
|
|
|
|
OH |
|
|
|
|
9 |
|
|
|
|
10 |
|
O |
|
|
|
HO |
O |
|
|
m |
HO |
|
|
||
HO |
|
|
|
|
|
HSO3O |
|
O |
OH |
|
O |
|
|
|
|
O |
O |
|
C15H31 |
|
|
|
||
|
|
|
|
n |
|
O |
OH |
|
|
|
|
OH |
|
|
Рис. 3. Строение 6,6'$дикориномиколата трегалозы (вверху) и диацилированных производных 2$сульфата трегалозы (внизу) (m = 1 или 3, n = 2–9) [21].
МИКРОБИОЛОГИЯ том 83 № 3 2014
274 |
ФЕОФИЛОВА и др. |
жены в составе марадолипидов у спящих личинок нематоды Caenorhabditis elegans. Это первые пред$ ставители 6,6'$диацилпроизводных трегалозы, вы$ деленные из животного организма [24].
Вирулентные микобактерии содержат также сульфогликолипиды, основой молекул которых служит 2$сульфат трегалозы. Прочие гидроксилы трегалозного остатка могут быть ацилированы пальмитиновой, стеариновой или более сложны$ ми кислотами, такими как фтиоцерановая или гидроксифтиоцерановая [21].
БИОСИНТЕЗ ТРЕГАЛОЗЫ
Биосинтез трегалозы в природе происходит несколькими способами [25]. В клетках дрожжей, базидиомицетов, насекомых и ряда других орга$ низмов дисахарид образуется либо из α$D$глю$ козилфосфата и D$глюкозы под действием фос$ форилазы трегалозы [26], либо из УДФ$глюкозы и глюкозо$6$фосфата с последующим дефосфо$ рилированием [27]. В некоторых бактериях обна$ ружен фермент, катализирующий внутримолеку$ лярную перегруппировку мальтозы в трегалозу [28]. Другие бактерии способны использовать в качестве исходного материала для образования трегалозы крахмал или мальтодекстрины. В этом случае вначале синтаза мальтоолигозилтрегалозы (MTSase) катализирует образование остатка тре$ галозы на восстанавливающем конце мальтооли$ госахарида, после чего происходит гидролиз под действием трегалогидролазы мальтоолигозилтре$ галозы (MTHase), приводящий к отщеплению трегалозы и освобождающий новый мальтооли$ госахарид для участия в следующей стадии анало$ гичного превращения [20, 30].
Широкие возможности разнообразного прак$ тического применения трегалозы привели к по$ явлению большой серии работ, направленных на обеспечение доступности этого дисахарида. По$ скольку химический синтез α,α$трегалозы слиш$ ком сложен [31], разрабатывались биотехнологи$ ческие способы ее производства. В принципе лю$ бой из упомянутых путей биосинтеза трегалозы можно было бы применить для ее биотехнологи$ ческого получения. При разработке биотехноло$ гии приходится учитывать множество дополни$ тельных факторов, таких как наличие сырья, до$ ступность и устойчивость ферментов, условия проведения реакции, способы выделения про$ дукта и т.д.
БИОЛОГИЧЕСКАЯ ФУНКЦИЯ ТРЕГАЛОЗЫ
Роль трегалозы в растениях
В прошлом столетии в учебниках по физиоло$ гии растений можно было прочитать, что этот ди$ сахарид у растений в норме отсутствует, но может
появиться в определенных условиях и свидетель$ ствует о наступающей гибели растения [32]. В настоящее время наличие трегалозы в растениях уже не вызывало сомнений, так этот дисахарид был обнаружен у представителей цветковых из се$ мейства миротамновых Myrothamnus flabellifolius и
травянистых споровых растений – Selaginella lepi< dophylla. Позже трегалозу обнаружили в растениях риса и табака, но в очень низких концентрациях – 10 мкг/г [33], и роль этого дисахарида “оставалась до конца не выясненной” [34]. Предполагается, что трегалоза выполняет протекторную функцию во время абиотического стресса и защите некото$ рых растений от ряда патогенов. В то же время это молекула с “двойным лицом” [34], например, трегалоза может дестабилизировать метаболизм крахмала, поэтому ее роль в процессах, связан$ ных со стрессом у растений, требует более тща$ тельных исследований.
Большинство сахаров, как например, наибо$ лее распространенная у растений сахароза, дей$ ствуют как сигнальные молекулы [35]. Данных, позволяющих заключить, что трегалоза также вы$ полняет сигнальную роль, на настоящий момент еще недостаточно. Трудность заключается в том, что этот дисахарид взаимодействует с фосфоли$ пидами липидного бислоя мембран и белками, которые представляют часть систем передачи клеточных сигналов. Следует учесть, что у ангид$ робиотических растений в достаточно весомых концентрациях помимо сахарозы и трегалозы присутствуют арбутин, метиларбутин и амигда$ лин, которые также могут играть защитную роль при стрессовых воздействиях. Кроме того, у рас$ тений дополнительным механизмом защиты мембран от обезвоживания является витрифика$ ция или переход в аморфное состояние, при кото$ ром образуется суперохлажденная жидкость с чрезвычайно малой вязкостью (glassy state). Очень важным моментом для переживания ана$ биоза является состояние мембран, при этом вы$ ходу организма из анабитического состояния способствует наличие в бислойной мембране фосфатидидхолина и сфингомиелина, в составе ацильных цепей которых содержатся насыщен$ ные жирные кислоты. В заключение следует под$ черкнуть, что изучение роли трегалозы и трегало$ зо$6$фосфата как в процессах передачи информа$ ции в клетках (гликокоде), так и в абиотическом и анабиотическом стрессах началось относительно недавно, и полученные данные требуют дальней$ шего подтверждения [34].
Функция трегалозы у бактерий
Арсенал используемых “совместимых осмо$ протекторов” у бактерий включает полиолы (ос$ новным является глицерин), сахара (сахароза, трегалоза), аминокислоты (пролин, глутамино$
МИКРОБИОЛОГИЯ том 83 № 3 2014
ТРЕГАЛОЗА: ОСОБЕННОСТИ ХИМИЧЕСКОГО СТРОЕНИЯ |
275 |
вая кислота) и четвертичные амины (глицинбе$ таин, эктоин, гидроксиэктоин) [36]. У галоалка$ лофильных бактерий наиболее распространены эктоин и глицинбетаин, у других прокариот – трегалоза, L$пролин и глицинбетаин. Однако каждый из протекторов выполняет свою опреде$ ленную функцию. Роль трегалозы очень важна при обезвоживании бактерий. Так, этот дисаха$ рид защищает мембраны Escherichia coli и спо$ собствует установлению их стекловидного состо$ яния при высушивании, причем этот процесс протекает без участия глицинбетаина [37]. Cинтез трегалозы индуцируется при выдерживании E. co< li при низкой температуре, и трегалоза необходи$ ма для выживания бактерий в условиях холода [38]. В то же время глицинбетаин, в отличие от трегалозы, не оказывает термопротекторного действия при тепловом шоке, но защищает белки при термоденатурации, действуя как стабилиза$ тор. Аналогичный эффект оказывает холин [39].
Роль трегалозы у грибов
Динамика содержания трегалозы у грибов в про8 цессе роста и в состоянии покоя. Жизненный цикл грибов (как и многих прокариот) можно условно разделить на два этапа: 1 – когда протекают ак$ тивные ростовые процессы, и происходит образо$ вание продуктов первичного метаболизма; 2 – за$ медление ростовых процессов, появление про$ дуктов вторичного метаболизма и переход к образованию покоящихся клеток. Оба этапа свя$ заны с процессом цитодифференцировки, на определении которой в ее современном понима$ нии следует особо остановиться. Цитодифферен$ цировку часто рассматривают как процесс, при$ водящий к специализации метаболизма клетки и ее функций. При этом дифференцировка не обя$ зательно является переходом от простого к слож$ ному, у организма одни свойства могут утрачи$ ваться, а другие усиливаться. Основным механиз$ мом цитодифференцировки в настоящее время принято считать дифференциальную экспрессию генов. Особенность дифференцировки клеток со$ стоит в том, что она необратимо приводит к опре$ деленному типу клеток, и этот процесс, находя$ щийся под контролем генов, называют детерми$ нацией. В ходе цитодифференцировки гены действуют в разное время, что выражается в тран$ скрипции различных мРНК, т.е. наблюдается ре$ прессия и дерепрессия генов. Особая роль в этом процессе принадлежит мРНК, хотя тРНК и рРНК также, но значительно меньше, влияют на проте$ кание процесса цитодифференцировки. Матри$ цы, регулирующие такую цитодифференцировку, как процесс споруляции, являются долгоживу$ щими, регулируются на уровне траскрипции, мо$ гут синтезироваться на ранних этапах развития организма и долгое время сохраняться в неактив$
ном состоянии, пока не поступит специальный сигнал из цитоплазмы, связанный с активацией деградации трегалозы.
Предполагают, что дифференциация и детер$ минация осуществляется на основе специаль$ ных клеточных сигналов [40], причем в комму$ никации грибов можно проследить тесную взаи$ мосвязь их коэволюции с мультивидовой коммуникацией, и этот процесс следует рас$ сматривать в контексте фундаментальных био$ логических функций, таких как рост, морфоге$ нез, половые взаимодействия и др.
Цитодифференцировка часто является резуль$ татом стресса (истощение среды и др.), и его дей$ ствие различается в зависимости от стадии разви$ тия организма. Поэтому, безусловно, полезно разделять стресс на запрограммированный и не$ запрограммированный [2]. Существенное разли$ чие между этими видами стресса состоит в том, что в первом случае организм уже подготовлен к переходу в состояние покоя, протеканию процес$ сов вторичного метаболизма и цитодифференци$ ровки, в том числе морфологической, проявляю$ щейся в образовании покоящихся клеток – спор. В случае незапрограммированного стресса про$ цесс цитодифференцировки мицелия практиче$ ски не выражен, бислойная мембрана имеет иной липидный состав и конечной целью антистрессо$ вых механизмов является переход к гомеостазу, а не к стадии покоя. Интересно, что при действии обоих видов стресса происходит синтез трегало$ зы, но дальнейшая судьба этого метаболита очень четко связана именно с видом стресса.
Методом ядерного магнитного резонанса (ЯМР) с использованием меченой 13С$трегалозы удалось установить, что в процессе прорастания асков дрожжей до 80% накопленной трегалозы превращается в глюкозу, которая, однако, не ис$ пользуется на ростовые процессы [41]. Оставши$ еся 20% трегалозы образуют особый пул, ком$ партментализованный в специальных клеточных отсеках. При добавлении меченой глюкозы пока$ зано, что именно она активно используется в про$ цессах прорастания покоящихся клеток, а не тре$ галоза. Более того, этот дисахарид активно убира$ ется из клеток при прорастании спор; трегалоза под действием фермента трегалазы распадается до глюкозы, а далее превращается в глицерин, ко$ торый достаточно быстро выводится из клеток. В то же время глюкоза, полученная из трегалозы под действием фермента трегалазы, используется как резерв углерода при хранении спор, находя$ щихся в состоянии экзогенного покоя. Из этих данных следует вывод, что в течение ростовых процессов, в частности, при прорастании споры, накопленная в ней трегалоза не используется, и активно в виде глицерина выводится из прораста$ ющей клетки. В то же время при хранении споро$
МИКРОБИОЛОГИЯ том 83 № 3 2014
276 |
ФЕОФИЛОВА и др. |
вого материала содержание трегалозы постепен$ но уменьшается, и она используется на поддержа$ ние экзогенного покоя. В этом процессе остается много неясного: в частности, зачем нужен остаю$ щийся в клетке специальный пул трегалозы, по$ чему при прорастании споры не используется глюкоза, образованная из трегалозы, но суть со$ стоит в том, что высокое содержание трегалозы в клетке несовместимо с ростовыми процессами (недаром этот дисахарид называют “сахаром по$ коя”).
При незапрограммированном стрессе, как пра$ вило, происходит быстрое образование трегалозы, и ее роль состоит в том, что этот дисахарид – анта$ гонист ростовых процессов, а при любом виде стресса организму необходимо остановить про$ цессы роста и пролиферации. В данном случае проще всего это сделать, удалив глюкозу, превра$ тив ее в трегалозу. Однако в последнее время по$ явились данные, свидетельствующие о том, что на$ копление трегалозы не всегда является стрессовым ответом [42]. Так, у мутантного штамма Saccharo< mycopsis fibuligera A11 с высоким содержанием тре$ галозы при различных стрессовых воздействиях не было выявлено ни активации трегалозофосфат$ синтетазы, ни изменения содержания трегалозы. Эти данные показывают, что еще далеко не все из$ вестно о функциональном значении трегалозы, и в этом отношении интерес представляют исследова$ ния термофильных грибов, у которых активный синтез трегалозы совпадает с активацией ростовых процессов [43], а не со стадией идиофазы.
Влияние трегалозы на вирулентность и димор8 физм грибов. В ряде работ показано влияние экзо$ генной трегалозы на характер роста (диморфизм) у мукоровых грибов [44, 45]. В условиях культиви$ рования, благоприятных для дрожжеподобного роста, в присутствии трегалозы наблюдалось раз$ витие грибов исключительно по мицелиальному типу, которое сопровождалось увеличением тре$ галазной активности [44] и повышенным уровнем полиненасыщенных жирных кислот (γ$линолено$ вой и арахидоновой) [45], что свидетельствует о влиянии трегалозы на реализацию морфогенети$ ческих программ у грибов.
Биосинтез трегалозы оказывает влияние не только на развитие грибов и стрессовый ответ, но и на вирулентность. Однако и в этом случае еди$ нообразной картины не наблюдается. Так, не$ смотря на то, что биосинтез трегалозы необходим для большого количества процессов, в том числе для проявления вирулентности у Cryptococcus gattii
(гены TPS1 и TPS2) [46] и Candida albicans (ген TPS1) [47], у Aspergillus fumigatus, патогена, кото$ рый вызывает инвазивные и часто фатальные ле$ гочные заболевания, нарушения в генах tpsAB (трегалозосинтаза), напротив, сопровождались увеличением вирулентности [48].
На модели мышиного системного кандидоза было показано, что у неспособных к росту на экзо$ генной трегалозе atc1 <мутантов Candida albicans (это ген кодирует кислую трегалазу, связанную с клеточной стенкой) снижалась способность к об$ разованию гиф и псевдогиф, а, следовательно, и вирулентность гриба [49].
Роль трегалозы в стабилизации и защите белков и мембран при обезвоживании. Состояние анабио$ за присуще многим организмам и характеризует$ ся в большинстве случаев потерей воды. Установ$ лено, что некоторые особи могут терять до 93% воды, например, коловратки, тихоходки и нема$ тоды, однако при появлении влаги происходит полное восстановление жизненных функций этих организмов. Было установлено, что многие организмы также могут пережить достаточную потерю воды: черви до 73%, черепахи – 53%, до$ машняя мышь – 30%, при этом, соответственно, снижается и время их нахождения в анабиозе [6]. При дегидратации микроорганизмов, в частно$ сти, дрожжей, как и при любом стрессе, отмечали быстрый синтез трегалозы [13, 50–54], причем этот процесс, вероятно, является универсальным, так как наблюдается даже у архей [55]. Но есть ис$ ключение – у растений в такой ситуации предпо$ чтительно используется другой дисахарид – саха$ роза, хотя трегалоза обладает меньшей способ$ ностью образовывать кристаллы, а процесс кристаллообразования опасен для организмов при обезвоживании и понижении температуры.
При обезвоживании организма трегалоза вы$ полняет роль стабилизатора белков и фосфоли$ пидов в липидном бислое. В этом процессе боль$ шое значение может иметь влияние трегалозы на микровязкость – интегральную величину, связан$ ную, в том числе, со степенью ненасыщенности ацильных цепей липидов. Установлено, что мик$ ровязкость повышается параллельно концентра$ ции в клетках трегалозы, и это оказывает влияние на складирование белков и активность ферментов [56]. Механизм биомолекулярной стабилизации изучался с использованием Фурье инфракрасной спектроскопии (FTIR) для характеристики взаи$ модействий между трегалозой, белками и сахара$ ми. В дальнейшем методы инфракрасной и рама$ новской спектроскопии позволили установить важную роль молекул трегалозы, которые концен$ трировали оставшуюся воду вблизи белков, что способствовало их стабилизации [26].
При стабилизации фосфолипидов роль трега$ лозы иная. Она взаимодействует с липидами пу$ тем образования водородных связей между ОН$ группами дисахарида (замещая при этом 10– 12 молекул воды) и полярными группами головок фосфолипидов, т.е. как бы заменяет удаленную при дегидратации воду и временно консервирует мембрану [12, 57]. Следует особо отметить, что
МИКРОБИОЛОГИЯ том 83 № 3 2014
ТРЕГАЛОЗА: ОСОБЕННОСТИ ХИМИЧЕСКОГО СТРОЕНИЯ |
277 |
при охлаждении и обезвоживании значительно возрастает степень ненасыщенности ацильных цепей липидов, которые становятся более уязви$ мыми в процессах перекисного окисления. В этом случае роль трегалозы более значима для стабилизации липидного бислоя по сравнению с ее близким химическим аналогом – сахарозой. Кроме того, потеря воды при обезвоживании приводит к изменениям в организации бислой$ ной структуры мембран, т.е. к увеличению темпе$ ратуры фазового перехода гель–жидкий кристалл (Tm), а для некоторых типов фосфолипидов – к образованию небислойных структур, при кото$ рых нормальное функционирование мембраны уже невозможно. В этом случае трегалоза эффек$ тивно предотвращает индуцированное дегидрата$ цией увеличение Tm за счет указанного выше вза$ имодействия с полярными головками фосфоли$ пидов [58].
Протекторные полиолы и трегалоза при стреccе у грибов
В настоящее время, кроме трегалозы, известен ряд соединений, способных осуществлять про$ текторную функцию при стрессе: глицерин, гли$ козилглицерин, арабит, маннит, сорбит (полио$ лы), а также аминокислоты глутамат, глицин, глицинбетаин, эктоин, гамма$аминомаслянная кислота, пролин, бетаин. В последние годы инте$ рес вызывают протекторные соединения нового класса, например, триметиламин$N$оксид. У грибов наиболее изучено влияние полиолов, осо$ бенно маннита и глицерина [59].
Угрибов биохимическая адаптация к темпера$ турному стрессу, обусловленная протекторами уг$ леводной природы, различается в зависимости от их систематического положения [59]. У предста$ вителей класса Zygomycetes – Cunninghamella japonica и Absidia coerulea работает только один биохимический механизм, основанный на превра$ щении глюкозы в дисахарид трегалозу. Последняя выполняет функцию стабилизатора мембранных липидов и является своеобразным “депо” такого высокоактивного субстрата, как глюкоза. Инте$ ресно, что только в условиях более глубокого (до 10°С) охлаждения появляются следы глицери$ на у представителей этих видов, а у (–) штамма Blakeslea trispora в стилоспорах, полученных в условиях гипертермии, обнаруживается полиол инозит.
Угрибов, принадлежащих к классу Ascomycet< es, в частности, Aspergillus japonicus и Myceliophtho< ra thermophila набор углеводов цитозоля более об$ ширен. Кроме трегалозы, имеется ряд полиолов, также выполняющих функцию протекторных со$ единений. При гипертермии отмечается тенден$ ция увеличения образования трегалозы и инози$
та, а при гипотермии – маннита и глицерина. На$ блюдается интересная особенность, связанная с температурным оптимумом роста организма. У термофила M. thermophila, имеющего оптимум роста при 41–42°С, глицерин не образуется при низкотемпературном шоке, но этот полиол появ$ ляется у мезофила A. japonicus, имеющего более низкий температурный оптимум роста.
Еще более широкий набор углеводных протек$ торов содержит цитозоль базидиомицетов. У этих грибов адаптация к температуре осуществляется с участием других биохимических механизмов. У Lentinula edodes при гипотермии в качестве крио$ протектора выступает арабит, а не маннит, как у аскомицетных грибов, но, как и у последних, об$ наруживается глицерин.
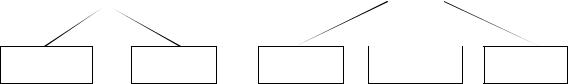
Учитывая температурные оптимумы плодоно$ шения исследуемых грибов в природных услови$ ях и приведенные выше данные, можно выска$ зать ряд предположений о функциональной роли углеводов цитозоля у базидиомицетов. Дополни$ тельную ценную в этом отношении информацию дали опыты по действию “холодового” шока на грибы L. edodes. С этой целью мицелий L. edodes, выращенный на твердой среде при 26–27°С, под$ вергали “холодовому” шоку (выдерживали 36 ч при 8–10°С). Понижение температуры культиви$ рования приводило к тому, что начинался про$ цесс образования примордиев, в которых преоб$ ладающим углеводом становился арабит, и содер$ жание этого полиола увеличивалось с 30 до 65%. При этом уровень маннита снижался незначи$ тельно, а количество трегалозы уменьшалось по$ чти в три раза. У базидиомицета Pleurotus ostreatus при гипертермии резко увеличивался уровень са$ харозы, и наблюдалось исчезновение арабита. Следует обратить внимание на тот факт, что в присутствии сахарозы наблюдались отличия в температурозависимом накоплении трегалозы. У всех исследованных грибов количество трегалозы снижалось при понижении температуры культи$ вирования, что можно объяснить тем, что в усло$ виях холода трегалоза может быстро превращать$ ся в глицерин, вследствие чего количество этого дисахарида уменьшалось. У P. ostreatus, вероятно, этот биосинтетический механизм отсутствует, и адаптация к температурному стрессу осуществля$ ется синергическим действием трегалозы и саха$ розы, причем их соотношение определяется ее повышением или понижением. Следовательно, появление в составе углеводов цитозоля сахарозы изменяет биохимические механизмы, регулирую$ щие адаптацию к гипо$ и гипертермии у базиди$ альных грибов. Можно предположить представ$ ленную на рис. 4 температурную зависимость синтеза углеводов у базидиомицетов.
Факт, что сахара цитозоля грибов несут опре$ деленную функциональную нагрузку, подтвер$
МИКРОБИОЛОГИЯ том 83 № 3 2014
278 |
|
ФЕОФИЛОВА и др. |
||||
|
|
|
|
|
|
|
|
|
|
|
Гипертермия |
||
|
Гипотермия |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Арабит |
Маннит |
Инозит |
Трегалоза |
Сахароза |
Рис. 4. Протекторные полиолы базидиальных грибов в условиях гипо$ и гипертермии.
ждают и другие данные. Очень интересным явля$ ется состав коричневой пленки L. edodes, которая появляется перед плодоношением и морфологи$ чески отличается от мицелия. В этом случае, как и в гифах поверхностного мицелия, преобладает глюкоза, но появляются два новых углевода – са$ хароза и неидентифицированный дисахарид. В спорах же L. edodes нет сахарозы, но практически в равном количестве присутствуют арабит, ман$ нит и трегалоза, т.е. спора как бы защищена от действия любой температуры протекторными со$ единениями. В базидиоспорах Pleurotus ostreatus кроме того появляются сахароза и инозит.
Эти данные позволяют предположить, что эволюция у грибов шла по линии синтеза больше$ го числа протекторных соединений углеводной природы и большей специализации их протек$ торных свойств. И если в спорах низших грибов, например, мукоровых, присутствует только тре$ галоза (у Cunninghamella japonica трегалоза состав$ ляет до 90 95% от суммы сахаров), то у аскомице$ тов появляются в качестве основных протекторов полиолы – эритрит, маннит и инозит, а у базидио$ мицетов, как и у растений, на определенных стади$ ях онтогенеза обнаруживается сахароза, способная замещать трегалозу и выполняющая, вероятно, еще какую$то дополнительную функцию в стабилиза$ ции липидного бислоя мембран [59].
Функция трегалозы как антиоксиданта
Установлено, что экзогенные неприродные антиоксиданты, например, 4,4$дикумилдифе$ нил$N$оксид, а также природные – α$токоферол, убихинон Q9, в том числе и собственные антиок$ сиданты грибов – обладают общим биологиче$ ским эффектом, стимулируют рост грибов, изме$ няют состав липидов, увеличивают степень их не$ насыщенности и содержание фосфатидилсерина [60], на фоне увеличения уровня трегалозы. Роль трегалозы как антиоксиданта была показана в опытах с Saccharomyces cerevisiae, клетки которых подвергали действию теплового шока или инги$ битора протеасомы (MG 132). При этом наблюда$ ли накопление трегалозы и увеличение жизне$ способности клеток дрожжей [61]. Известно, что
этанол, как токсический продукт, вызывает сво$ боднорадикальное повреждение липидов клеточ$ ных структур и дегидратацию. Увеличение его концентрации в среде также сопровождается воз$ растанием уровня трегалозы [51, 53, 54]. Ранее бы$ ли получены данные о том, что процесс клеточно$ го деления в культуре клеток и тканей высших эу$ кариот связан не только с количеством антиоксидантов, но и составом липидов мембран, степенью их ненасыщенности и их антиокисли$ тельной активностью. Эти же закономерности бы$ ли подтверждены в опытах с прокариотами и низ$ шими эукариотами, в том числе с мицелиальными грибами [62]. В этих исследованиях была установ$ лена взаимосвязь между степенью ненасыщенно$ сти ацильных цепей липидов, микровязкостью липидного бислоя мембран и интенсивностью накопления трегалозы в мицелии грибов. Эти данные свидетельствовали об антиоксидантных свойствах трегалозы.
Есть сведения о действии трегалозы как про$ тектора жирных кислот в модельных системах [63]. Оно выражается в предотвращении (1) дегра$ дации ненасыщенных линолевой и α$линоленовой кислот с образованием альдегидов и (2) автоокис$ ления ненасыщенных жирных кислот с образова$ нием пероксидов. На основании этого был сделан вывод о прямом взаимодействии трегалозы с ацильными цепями и стабилизации структуры ЖК [63]. Механизм защитного действия трегалозы про$ тив свободнорадикального окисления липидов был подтвержден в 2003 г. Используя метод ЯМР, были получены спектры H1 и C13, позволяющие судить о
взаимодействии OH…π и CH…O между трегалозой и ненасыщенными жирными кислотами. Трегалоза значительно снижала действие свободнорадикаль$ ного окисления на ненасыщенные ацилы липидов путем слабого связывания с двойными связями в молекулах жирных кислот [64].
ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ И ПРАКТИЧЕСКОЕ ИСПОЛЬЗОВАНИЕ
ТРЕГАЛОЗЫ
Для препаративного получения сравнительно небольших количеств трегалозы предложена экс$
МИКРОБИОЛОГИЯ том 83 № 3 2014
|
|
ТРЕГАЛОЗА: ОСОБЕННОСТИ ХИМИЧЕСКОГО СТРОЕНИЯ |
|
279 |
|||||||
тракция биомассы пекарских дрожжей [18], со$ |
|
100 |
|
|
ВКМ F$921(–) |
||||||
держащих около 20% этого дисахарида. Процесс |
|
90 |
|
|
ВКМ F$904(+) |
||||||
ферментации и условия хранения дрожжей были |
|
|
|
||||||||
|
80 |
|
|
|
|
||||||
досконально разработаны еще в конце ХХ столе$ |
% |
|
|
ВКМ F$903(–) |
|||||||
тия рижскими учеными [6]. Было показано, что |
спор, |
70 |
|
|
ВКМ F$666(+) |
||||||
клетки дрожжей с высоким содержанием трегало$ |
|
|
|
||||||||
60 |
|
|
|
|
|||||||
зы (10–16%) хорошо сохраняют жизнеспособ$ |
Проросших |
50 |
|
|
|
|
|||||
ность во время длительного хранения. |
|
|
|
|
|||||||
|
|
|
|
|
|||||||
Крупномасштабное промышленное получе$ |
40 |
|
|
|
|
||||||
30 |
|
|
|
|
|||||||
ние этого дисахарида осуществляется биотехно$ |
|
|
|
|
|||||||
20 |
|
|
|
|
|||||||
логическими методами, основанными на фер$ |
|
|
|
|
|||||||
|
|
|
|
|
|||||||
ментативных превращениях крахмала [19]. Осу$ |
|
10 |
|
|
|
|
|||||
ществленный в Японии промышленный процесс |
|
0 |
|
|
|
|
|||||
использует в качестве исходного материала крах$ |
|
7 |
14 |
21 |
28 |
||||||
|
0 |
||||||||||
мал кукурузы или тапиоки, который предвари$ |
|
||||||||||
|
|
|
Сутки |
|
|
||||||
тельно обрабатывают α$амилазой, изоамилазой и |
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
рядом других ферментов для получения смеси не$ |
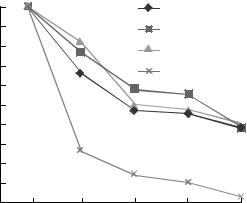
Рис. 5. Прорастание спор B. trispora при хранении в |
||||||||||
разветвленных мальтоолигосахаридов, которую |
|||||||||||
воде. |
|
|
|
|
|||||||
далее превращают в трегалозу совместным дей$ |
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
ствием MTSase и MTHase. Имеющееся производ$ |
|
|
|
|
|
|
|||||
ство позволило уже к 2005 году вырабатывать еже$ |
розой, в молекуле которой остаток β$D$фруктозы |
||||||||||
годно около 30000 т дигидрата трегалозы с чисто$ |
находится в фуранозной форме. |
|
|
||||||||
той 98% [65]. Последующие предложения по |
В ряде случаев трегалоза может быть более |
||||||||||
усовершенствованию процесса сводятся к освое$ |
|||||||||||
нию новых источников сырья, новых приемов |
эффективным криопротектором для хранения |
||||||||||
очистки трегалозы и к утилизации образующихся |
коллекционных и промышленных культур мик$ |
||||||||||
побочно продуктов в виде биоэтанола или глюко$ |
роорганизмов, чем традиционно используемый |
||||||||||
новой кислоты [66, 67]. В настоящее время более |
глицерин. |
|
|
|
|
||||||
передовым считаются новые методы фермента$ |
Cогласно нашим данным, приведенным на |
||||||||||
тивной биотрансформации, в основе которой ле$ |
|||||||||||
рис. 5 и 6, споры трех из 4$х изученных производ$ |
|||||||||||
жат три основных пути синтеза трегалозы: фосфо$ |
|||||||||||
ственных штаммов$продуцентов каротина Blakes< |
|||||||||||
рилазная система, обнаруженная у мицелиальных |
|||||||||||
lea trispora сохраняли высокую степень жизнеспо$ |
|||||||||||
грибов и дрожжей, гликозилтрансферазно$гидро$ |
|||||||||||
собности при хранении в воде при комнатной |
|||||||||||
лазная система, свойственная мезофильным бак$ |
|||||||||||
температуре в течение месяца. Только жизнеспо$ |
|||||||||||
териям Arthrobacter sp., и синтез трегалозы из маль$ |
|||||||||||
собность спор у штамма ВКМ F$666(+) относи$ |
|||||||||||
тозы, |
катализируемый |
интрамолекулярным |
|||||||||
тельно других штаммов в конце эксперимента |
|||||||||||
трансгликозилированием (Thermus |
ssp.) [26]. В |
||||||||||
снижалась в 10 раз. При отрицательных темпера$ |
|||||||||||
1990 г. стоимость 1 кг трегалозы составляла почти |
|||||||||||
турах для хранения культур грибов используются |
|||||||||||
$700, в настоящее время благодаря новым техно$ |
|||||||||||
протекторы, среди которых, как уже было отме$ |
|||||||||||
логиям стоимость этого дисахарида значительно |
|||||||||||
чено, |
наиболее |
распространен |
глицерин. |
Из |
|||||||
снизилась. |
|
|
|
||||||||
|
|
|
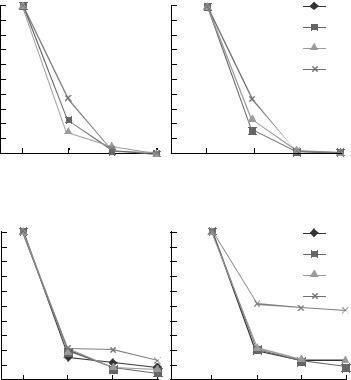
рис. 6а видно, что при температуре –12°С проис$ |
||||||||
|
|
|
|
|
|||||||
Наиболее широко трегалоза используется при |
ходит резкое падение прорастания спор в услови$ |
||||||||||
хранении пищевых |
продуктов, биоматериалов, |
ях эксперимента (картофельно$глюкозная среда, |
|||||||||
вакцин в условиях комнатных температур, предо$ |
5 ч, 25°С) вне зависимости от характера протекто$ |
||||||||||
хранении ферментов от разрушения и для защиты |
ра. Однако, в случае использования в качестве |
||||||||||
клеток, в т.ч. клеток млекопитающих от повре$ |
криопротектора трегалозы, через трое суток на |
||||||||||
ждений при низкотемпературной сушке [68]. Тре$ |
чашках Петри, в которые помещали споры для |
||||||||||
галоза применяется в косметике как стабилизатор |
оценки прорастания, был отмечен рост мицелия |
||||||||||
липосом и в пищевой индустрии – при внесении |
и обильное формирование спорогенного аппара$ |
||||||||||
подсластителей. При стабилизации подсластите$ |
та. При хранении штаммов в присутствии глице$ |
||||||||||
лей трегалоза, в отличие от других сахаров, не |
рина все они полностью теряли жизнеспособ$ |
||||||||||
вступает в химические реакции с аминокислота$ |
ность. Оценка степени сохранения жизнеспособ$ |
||||||||||
ми и белками и не приводит к появлению корич$ |
ности спор после хранения при температуре – |
||||||||||
невой окраски. Объясняется это тем, что в моле$ |
70°С показала, что и в этом случае трегалоза |
||||||||||
куле трегалозы отсутствует свободная альдегид$ |
была более предпочтительна в качестве криопро$ |
||||||||||
ная группа, а гликозидная связь, соединяющая |
тектора для культур B. trispora по сравнению с |
||||||||||
два α$D$глюкопиранозных остатка, обладает по$ |
глицерином. Так, через 60 сут хранения с этим |
||||||||||
вышенной устойчивостью по сравнению с саха$ |
криопротектором степень прорастания спор была |
||||||||||
МИКРОБИОЛОГИЯ |
том 83 |
№ 3 |
2014 |
|
|
|
|
|
|
||
280 |
|
|
|
ФЕОФИЛОВА и др. |
|
|
||
|
|
|
|
(a) |
|
|
|
|
|
100 |
Глицерин |
|
|
Трегалоза |
|
ВКМ F$921(–) |
|
% |
90 |
|
|
|
|
|
|
ВКМ F$904(+) |
80 |
|
|
|
|
|
|
||
спор, |
|
|
|
|
|
|
ВКМ F$903(–) |
|
70 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
Проросших |
60 |
|
|
|
|
|
|
ВКМ F$666(+) |
50 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
0 |
1 |
15 |
60 |
0 |
1 |
15 |
60 |
|
0 |
|||||||
|
|
|
|
Сутки |
|
|
|
|
|
|
|
|
(б) |
|
|
|
|
|
100 |
Глицерин |
|
|
Трегалоза |
|
ВКМ F$921(–) |
|
% |
90 |
|
|
|
|
|
|
ВКМ F$904(+) |
80 |
|
|
|
|
|
|
||
спор, |
|
|
|
|
|
|
ВКМ F$903(–) |
|
70 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
Проросших |
60 |
|
|
|
|
|
|
ВКМ F$666(+) |
50 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
0 |
1 |
15 |
60 |
0 |
1 |
15 |
60 |
|
0 |
|||||||
|
|
|
|
Сутки |
|
|
|
|
Рис. 6. Прорастание спор B. trispora при хранении с протекторами при температуре –12°С (а) и –70°С (б).
в 1.5–3 раза выше, чем в присутствии глицерина, особенно в случае штамма ВКМ F$666(+).
Благодаря своим уникальным протекторным свойствам трегалоза в настоящее время начинает все шире использоваться в медицине. Уже извест$ ны несколько препаратов – Авастин, Герцептин (“Roche”), Адвате (“Baxter”), Луцентис (“Novar$ tis”), которые подтверждают необходимость ис$ пользования трегалозы как ингредиента лекар$ ственных препаратов. Трегалоза используется как компонент в растворе Kyoto для сохранения ткани панкреатической железы при трансплантации. Трегалоза также более эффективна, чем растворы гидроксицеллюлозы и гиалуронана, для защиты глаз при их обезвоживании (при длительном чте$ нии). В последнем случае трегалоза защищает клетки эпителия роговицы от синдрома “сухих глаз” и действия свободных радикалов (окисли$ тельный инсульт глаза) [69]. В последние годы ис$ пользование трегалозы в офтальмологии расширя$ ется [3]. Положительный эффект от применения трегалозы обнаруживают при лечении все больше$ го числа заболеваний, например, хореи Хантинг$ тона и болезни Альцгеймера. Относительно недав$ но трегалоза и продукты ее метаболизма нашли
применение в растениеводстве. Так, ген, кодирую$ щий фосфорилазу трегалозы (TP) и полученный из Pleurotus sajor<caju использовали в работах по инже$ нерии растений табака. Полученное генно$инже$ нерное растение аккумулировало трегалозу и при$ обретало устойчивость к дефициту воды по сравне$ нию с дикими штаммами табака. Это направление в биоинженерии растений – использование трега$ лозы в условиях абиотического стресса – приобре$ тает все большую популярность [70].
В заключение следует сказать, что природа со$ здала молекулу, уникальную по своему химиче$ скому строению и биологическим свойствам, на$ значение которой – сохранять жизнь практиче$ ски при любых неблагоприятных условиях.
СПИСОК ЛИТЕРАТУРЫ
1.Wiggers H.A.L. Untersuchung über das Mutterkorn, Secale cornutum // Ann. Pharmacie. 1832. V. 1. № 2. P. 129–182.
2.Феофилова Е.П. Трегалоза, стресс и анабиоз // Микробиология. 1992. Т. 61. № 5. С. 741–753. Feofilova E.P. Trehalose, stress, and anabiosis // Mi$ crobiology. 1992. V. 61. № 5. P. 513–523.
МИКРОБИОЛОГИЯ том 83 № 3 2014
