

МЕДИЦИНСКОЕ ОБРАЗОВАНИЕ
Кафедра биологической и общей химии
БЕЛКИ
И
ФЕРМЕНТЫ
Учебно-методическое пособие для студентов лечебного факультета
к практическим занятиям по биологической химии
Под редакцией
проф. В.А. Дадали, доц. Р.Н. Павловой
Санкт-Петербург Издательство СЗГМУ им. И.И. Мечникова
2013
УДК 577.1(076.5)
Белки и ферменты : учебно-методическое пособие для студентов лечебного факультета к практическим занятиям по биологической химии ; изд. 3-е, перераб. и доп. / под ред. проф. В.А. Дадали, доц. Р.Н. Павловой. – СПб. : Изд-во СЗГМУ им. И.И. Мечникова, 2013. – 104 с.
Составители:
сотрудники кафедры биологической и общей химии СЗГМУ им. И.И. Мечникова О.А. Агафонова, Ж.В. Антонова, Ч.Р. Бейшебаева,
Н.Э. Голованова, Л.В. Иванова, В.А. Кулеба, М.Н. Макарова, Е.Б. Мирошникова, Р.Н. Павлова, М.Н. Смертина, Е.А. Соколова
Учебно-методическое пособие предназначено для студентов лечебного факультета медицинских вузов, выполняющих практические занятия по курсу биологической химии. В пособии перечислены компетенции, в освоении которых необходимы знания биологической химии, сформулированы цель и мотивация каждой темы, представлены вопросы для самоподготовки, основная и дополнительная литература к каждой теме, методика проведения практической работы, клинико-диагностическое и медикопрофилактическое значение определяемых показателей. После каждой темы приведены обучающие тесты с ответами, часть занятий изложена в виде ситуационных задач, для решения которых студенты пользуются дополнительной литературой, предлагаемой на занятии.
Утверждено в качестве учебного пособия методическим советом ГБОУ ВПО СЗГМУ им. И.И. Мечникова, протокол № 3 от 01 марта 2013 г.
|
УДК 577.1(076.5) |
ISBN 5-7243-0283-7 |
© Коллектив авторов, 2013 |
|
© Издательство СЗГМУ им. И.И. Мечникова, |
|
2013 |
ВВЕДЕНИЕ
К числу важных и актуальных проблем современной медицины относится разработка принципов диагностики и патогенетической терапии различных заболеваний, защиты организма от вредных воздействий внешней среды.
XXI век характеризуется появлением или увеличением тяжести так называемых болезней цивилизации – атеросклероза и других сердечнососудистых заболеваний (ИБС, инфаркт, инсульт), диабета, иммунодефицитов, увеличением числа заболеваний онкологической природы, повышенной нервно-эмоциональной нагрузки и стрессов и др. Усугубляется действие техногенных факторов, прежде всего многочисленных чужеродных веществ, электромагнитных и других полей, вибрации, повышенной радиации, иных излучений и т. д.
Если в основе жизнедеятельности лежит совокупность специфических превращений веществ и энергии, то функциональные и структурные нарушения, развивающиеся в живой системе под влиянием повреждающих факторов, следует рассматривать прежде всего как результат взаимодействия последних с жизненно важными субстратами клеток и тканей, как следствие торможения, дезорганизации или прекращения внутриклеточных процессов обмена веществ и энергии.
Изучение биохимического механизма действия патогенных факторов является необходимым элементом исследований, создающих научную основу для разработки способов ранней лабораторной диагностики, рациональной патогенетической терапии и профилактики заболеваний, вызываемых этими факторами. Все эти задачи в той или иной мере всегда возникают в поле зрения врача.
Биохимические исследования проводятся в современной клинике в широком масштабе при постановке диагноза и выборе тактики лечения. Они играют фундаментальную роль в разработке новых методов лечения, соответствующих лекарственных препаратов и создании природных рецептур лечебно-профилактического действия, а также разработке современных схем лечебного питания. Особое значение приобретает понимание функции основных метаболических систем, ферментных систем биотрансформации лекарственных препаратов и ксенобиотиков, антиоксидантных систем.
Биохимические исследования проводятся при изучении условий труда человека в разнообразных условиях его производственной дея-
3
тельности, поскольку с их помощью удается выявить ранние, скрытые признаки развития в организме патологического процесса, вызванного действием агентов, специфических для данного производства, конкретизировать причины патологических изменений и разработать на этой основе, учитывая результаты физиологических, гематологических и клинических исследований, рациональные мероприятия, гарантирующие в дальнейшем сохранение здоровья работников данного производства.
Поскольку развитию функциональных изменений, характерных для патогенного фактора, предшествуют метаболические сдвиги, их выявление с помощью разнообразных биохимических методов в большой мере способствует успешному решению упомянутой задачи.
Непосредственно связана с биохимическими концепциями и методами современная наука о рациональном питании здорового и больного человека. Качественная и количественная характеристика химического состава продуктов питания, данные о содержании в этих продуктах белков, углеводов, липидов, витаминов, минеральных веществ и других микронутриентов, их превращениях в организме при различных функциональных состояниях последнего и в различных условиях – эти и другие вопросы подобного рода, специфичные для гигиены питания, решаются на биохимической основе.
Изучение биологической химии, как одной из фундаментальных дисциплин в ряду других предметов при подготовке специалиста квалификации «врач» по специальности лечебное дело, направлено на овладение обучающимися следующими общекультурными (ОК) и профессиональными (ПК) компетенциями:
–ОК-1 – способностью и готовностью анализировать социальнозначимые проблемы и процессы, использовать на практике методы гуманитарных, естественно-научных, медико-биологических и клинических наук в различных видах профессиональной и социальной деятельности;
ОК-3 – способностью и готовностью к анализу значимых политических событий и тенденций, к ответственному участию в политической жизни, к овладению основными понятиями и закономерностями мирового исторического процесса, к уважительному и бережному отношению к историческому наследию и традициям, к оценке политики государства; знать историко-медицинскую терминологию;
–ОК-5 – способностью и готовностью к логическому и аргументированному анализу, к публичной речи, ведению дискуссии и полемики,
4
к редактированию текстов профессионального содержания, к осуществлению воспитательной и педагогической деятельности, к сотрудничеству и разрешению конфликтов, к толерантности;
–ПК-2 – способностью и готовностью выявлять естественнонаучную сущность проблем, возникающих в ходе профессиональной деятельности, использовать для их решения соответствующий физикохимический и математический аппарат;
–ПК-3 – способностью и готовностью к формированию системного подхода к анализу медицинской информации, опираясь на всеобъемлющие принципы доказательной медицины, основанной на поиске решений с использованием теоретических знаний и практических умений
вцелях совершенствования профессиональной деятельности;
–ПК-5 – способностью и готовностью проводить и интерпретировать опрос, физикальный осмотр, клиническое обследование, результаты современных лабораторно-инструментальных исследований, морфологического анализа биопсийного, операционного и секционного материала, написать медицинскую карту амбулаторного и стационарного больного;
–ПК-8 – способностью и готовностью проводить судебно-медицин- ское освидетельствование живых лиц; трактовать результаты лабораторных исследований объектов судебно-медицинской экспертизы в случае привлечения к участию в процессуальных действиях в качестве специалиста или эксперта;
–ПК-9 – способностью и готовностью к работе с медико-техниче- ской аппаратурой, используемой в работе с пациентами, владеть компьютерной техникой, получать информацию из различных источников, работать с информацией в глобальных компьютерных сетях; применять возможности современных информационных технологий для решения профессиональных задач;
–ПК-15 – способностью и готовностью к постановке диагноза на основании результатов биохимических исследований биологических жидкостей и с учетом законов течения патологии по органам, системам и организма в целом;
–ПК-16 – способностью и готовностью анализировать закономерности функционирования отдельных органов и систем, использовать знания анатомо-физиологических основ, основные методики клиникоиммунологического обследования и оценки функционального состояния;
–ПК-17 – способностью и готовностью выявлять у пациентов основные патологические симптомы и синдромы заболеваний, используя
5
знания основ медико-биологических и клинических дисциплин с учетом законов течения патологии по органам, системам и организма в целом, анализировать закономерности функционирования различных органов и систем при различных заболеваниях и патологических процессах, использовать алгоритм постановки диагноза (основного, сопутствующего, осложнений) с учетом Международной статистической классификации болезней и проблем, связанных со здоровьем (МКБ), выполнять основные диагностические мероприятия по выявлению неотложных и угрожающих жизни состояний;
–ПК-18 – способностью и готовностью анализировать и интерпретировать результаты современных диагностических технологий по воз- растно-половым группам пациентов с учетом их физиологических особенностей организма человека для успешной лечебно-профилакти- ческой деятельности, провести диагностику физиологической беременности, участвовать в проведении судебно-медицинской экспертизы;
–ПК-31 – способностью и готовностью изучать научно-медицин- скую информацию, отечественный и зарубежный опыт по тематике исследования;
–ПК-33 – способностью и готовностью к участию в освоении современных теоретических и экспериментальных методов исследования
сцелью создания новых перспективных средств, в организации работ по практическому использованию и внедрению результатов исследований.
6
Тема 1. СТРОЕНИЕ И СВОЙСТВА АМИНОКИСЛОТ. МЕТОДЫ ИССЛЕДОВАНИЯ АМИНОКИСЛОТ
Место проведения: кафедра биохимии. Продолжительность занятия – 180 мин.
Цель занятия: систематизировать знания о строении и свойствах аминокислот, необходимые для оценки физико-химических свойств и биологической роли белков. Обсудить различные методы исследования белков и идентификации аминокислот.
Конкретные задачи.
Студент должен знать:
–классификацию и строение аминокислот;
–физико-химические свойства аминокислот;
–роль аминокислот в организме. Студент должен уметь:
–написать формулу пептида в общем виде;
–использовать цветные реакции на белки в диагностической прак-
тике;
–анализировать результаты хроматографического разделения. Мотивация. Знания и навыки, приобретенные на занятии, необхо-
димы для оценки результатов санитарно-гигиенических исследований и в клинико-диагностической практике врача.
Изучение темы должно способствовать формированию общекультурных (ОК-5) и профессиональных (ПК-9, ПК-15) компетенций.
Задание для самоподготовки: изучить рекомендуемую литературу, используя вопросы для самоподготовки.
Рекомендуемая литература
Основная
Березов, Т.Т. Биологическая химия / Т.Т. Березов, Б.Ф. Коровкин. – М. :
Медицина, 1998. – С. 27–43, 53–56, 74–77.
Биохимия : учебник для вузов / под ред. проф. Е.С. Северина. – М. :
ГЭОТАР-МЕД, 2003. – С. 10–19; То же. – 2011. – С. 1–19.
Белки и ферменты : учебно-методическое пособие к практическим заняти-
ям по биологической химии / под ред. проф. В.А. Дадали, доц. Р.Н. Павловой. – СПб. : Изд-во СЗГМУ им. И.И. Мечникова, 2013.
Дополнительная
Марри, Р. Биохимия человека ; т. 1 / Р. Марри, Д. Греннер, П. Мейес, В. Ро-
дуэлл. – М. : Мир, 1993. – С. 21–41.
7
Кальман, Я. Наглядная биохимия / Я. Кальман. – М. : Мир, 2000. – С. 64–68. Лабораторные методы исследования в клинике / под ред. В.В. Мень-
шикова. – М. : Медицина, 2002.
Вопросы для самоподготовки
1.Какова роль аминокислот в организме?
2.Что такое заменимые и незаменимые аминокислоты? Приведите примеры.
3.Приведите примеры производных аминокислот и охарактеризуйте их роль.
4.На чем основана классификация аминокислот? Приведите примеры и напишите структурные формулы аминокислот; дайте характеристику функциональных групп аминокислот.
5.Напишите пептид, содержащий полярные и неполярные радикалы аминокислот.
6.Что такое радикал аминокислоты и какова его роль в формировании белковой молекулы?
7.Приведите примеры биологически важных пептидов и охарактеризуйте их роль в организме.
8.Какие физико-химические свойства присущи аминокислотам?
9.Какие методы используются для исследования пептидов и аминокислот? Приведите примеры различных типов гидролиза.
10.Какие методы используются для определения N и C – концевых аминокислот? В чем заключается их принцип?
11.Какие цветные реакции на белки относятся к универсальным и почему?
12.Какие цветные реакции на белки относят к специфическим и почему? Приведите примеры специфических реакций.
13.Каково значение использования цветных реакций в практике
врача?
14.Какие виды хроматографии вам известны?
15.На чем основан метод распределительной бумажной хроматографии?
16.С какой целью используют различные виды хроматографии?
ЛАБОРАТОРНАЯ РАБОТА
Цветные реакции на белки
Цель работы: используя цветные реакции на белки, обнаружить белок в растворе. Открыть функциональные группы исследуемых ами-
8

нокислот. УИРС – на основании полученных данных сделать заключение об аминокислотном составе и полноценности двух белков – яичного и желатины.
Проведение цветных реакций основано на образовании окрашенных соединений в результате взаимодействия того или иного реактива с определенными функциональными группами, входящими в состав молекулы белка.
Существует два типа цветных реакций:
1.Универсальные – биуретовая (характерна для всех белков и доказывает наличие пептидной связи) и нингидриновая (определяет наличие NH2-группы в α-положении у аминокислот и белков).
2.Специфические реакции, характерные для отдельных аминокислот, содержащих специфические функциональные группы.
Универсальные реакции на белки
Биуретовая реакция. В результате взаимодействия ионов двухвалентной меди с пептидными связями в щелочной среде образуется комплексное соединение, окрашенное в красно-фиолетовый цвет. Название реакции обусловлено тем, что биурет (продукт конденсации двух молекул мочевины NH2–CO–NH–CO–NH2) в аналогичных условиях дает такой же комплекс.
|
|
|
R |
|
|
|
|
|
|
|
|
R |
1 |
|
|
|
|
|
R 2 |
|
|
R |
|
|
|
|
|
R1 |
|
|
|
R |
2 |
||||||||||||||||||||||
N |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
CH |
|
|
C |
|
N |
|
|
CH C |
|
|
N |
|
|
CH |
|
|
|
|
|
|
N CH C |
|
|
N CH |
|
C |
|
N |
|
|
CH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
–2Н2О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ Cu |
|
Cu |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
O |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
CH |
|
C N |
|
CH C |
|
N |
|
CH |
|
|
|
|
|
N C |
|
HC |
|
N |
|
C CH N |
|
C |
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
||||
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
R |
1 |
|
|
|
|
R 2 |
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
пептидные связи в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
биуретовый |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
енольной форме |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
комплекс |
|
|
|
|
|
|
|||||||||||||||||||||||||||||
Проведение реакции: к 4–5 каплям раствора белка добавляют 5 капель 10 % раствора NaOH и 1 каплю (избыток мешает чтению результатов реакции!) 1 % раствора CuSO4. Так же проводят реакцию с желатиной.
9
Специфичность реакции: реакцию дают все соединения, содержащие в молекуле две и больше двух близко расположенных пептидных связей. Реакция характерна для всех белков (как полипептидов), но не специфична для них.
Реакция с нингидрином. Основана на его взаимодействии со свободной аминогруппой.
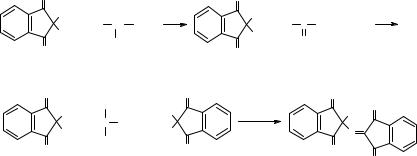
Механизм реакции: нингидрин, являясь сильным окислителем, вызывает отщепление аминогруппы с образованием свободного аммиака, СО2, альдегида и восстановленной формы нингидрина. Восстановленная форма нингидрина, реагируя с аммиаком и избытком нингидрина, дает продукт конденсации фиолетового цвета.
O |
|
|
|
O |
|
|
OH |
|
|
|
H |
|
|
+ |
R |
CH |
COOH |
+ R |
C H + NH3 + CO2 |
|
OH |
|
NH2 |
|
OH |
O |
|
O |
|
|
O |
|||
|
|
|
|
|||
O |
H |
|
O |
|
O |
|
H |
|
HO |
- 3 H2O |
H O |
||
N |
H |
|||||
+ |
+ |
|
|
|||
OH |
H |
|
HO |
|
N |
|
O |
|
O |
|
O |
||
|
|
|
O
Проведение реакции: к 4–5 каплям раствора белка добавляют 5 капель раствора нингидрина и длительно (5–10 мин) нагревают на кипящей водяной бане. Присутствующий аммиак должен быть удален из системы. Аналогичным образом проводят реакцию с желатиной.
Специфичность реакции: в реакцию вступают белки, пептиды, свободные аминокислоты и их производные.
Специфические реакции на отдельные аминокислоты и аминокислоты, входящие в состав молекулы белка или полипептида
Ксантопротеиновая реакция. Происходит при условии наличия в молекуле белка радикалов циклических аминокислот.
Механизм реакции: при действии на белок концентрированной азотной кислоты (белок при этом выпадает в осадок – см. раздел «Денатурация белков») происходит нитрование циклических (содержащих
10
