
3 курс / Патологическая физиология / Воспаление
.pdf
Medicine Books (https://vk.com/medicinebook)
Глава 3. Воспаление и репарация
I.Острое воспаление (ОВ)
1.Определение ОВ
1.1.Определение – кратковременный и ранний ответ на повреждение, характеризующийся высвобождением химических медиаторов и ведущий к типовому ответу со стороны сосудов мелкого калибра и лейкоцитов;
1.2.Не является синонимом инфекционного процесса.
2.Основные проявления воспаления (рис. 3.1):
2.1.Rubor и calor – краснота и местное повышение температуры, обусловленные гистамининдуцированным расширением сосудов;
2.2.Tumor – припухлость:
Благодаря гистамин-индуцированному расширению артериол;
Механизмы схожи с образованием обычного отека, в связи с повышением количества жидкости в интерстициальном пространстве.
2.3.Dolor – боль, связанная с простагландином Е2 (PGE2), способным повышать чувствительность специальных нервных окончаний к воздействию брадикинина и других болевых медиаторов;
2.4.Functio leasa – нарушение функции.
3.Этиология ОВ
3.1.Различные инфекции (вирусные или бактериальные);
3.2.Иммунологические реакции (н. реакция на укус пчелы);
3.3.Другие факторы, включающие: тканевой некроз (острый инфаркт миокарда), травматические повреждения, ожоги и обморожения, воздействие инородных тел (н. деревянная заноза и т.д.).
4.Последовательность сосудистых реакций при ОВ
4.1.Вазоконстрикция артериол, возникает рефлекторно и продолжается несколько секунд;
4.2.Вазодилятация артериол
Гистамин и другие вазодилятаторы (н. оксид азота) вызывают расслабление гладких мышц сосудистой стенки и, тем самым, увеличивают кровоток в сосуде. Как правило, гистамин высвобождается из тучных клеток, которые расположены в интерстиции вокруг небольших сосудов (рис. 3-2).
Увеличение кровотока в сосуде приводит к росту гидростатического давления (ГД) в просвете венул.
4.3.Повышение венозной проницаемости
Гистамин и другие медиаторы вызывают сокращение эндотелиоцитов в венулах, что приводит к появлению между клетками промежутков и обнажению базальной мембраны. Почему именно в венулах? Межклеточные связи у эндотелиальных клеток в венулах слабее, чем в артериолах.
Транссудат (жидкость с пониженным содержанием белков и клеток) проходит через интактную базальную мембрану в интерстициальное пространство за счет повышения ГД.
4.4.Отек ткани (припухлость). Лимфатические сосуды не справляются с отводом избытка интерстициальной жидкости, что и приводит к отеку ткани.
4.5.В конечном итоге, происходит снижение кровотока, что связано со сдавлением сосудов отечной жидкостью.
5.Последовательность клеточных реакций при ОВ (рис. 3-3), в первую очередь, описана для нейтрофилов на примере бактериальной инфекции.
5.1.Нейтрофилы являются главным действующим звеном при ОВ (рис. 3-4)
В циркулирующей крови, нейтрофилы разделены на циркулирующий пул и краевой пул, прикрепленный к эндотелию;

Medicine Books (https://vk.com/medicinebook)
Рис 3-1: Признаки острого воспаления (ОВ). У |
Рис 3-2: Электронная микрофотография тучной |
|||||||
новорожденного |
наблюдается |
врожденное |
клетки. В цитоплазме видно большое количество |
|||||
инфицирование Staphylococcus aureus. Симптомы ОВ |
гранул, |
содержащих |
гистамин, |
фактор |
||||
на фотографии: покраснение кожи, небольшой отек |
хемотаксиса |
эозинофилов |
и |
другие |
||||
вокруг кожных везикул. Помимо этого, наблюдается |
воспалительные медиаторы |
|
|
|
||||
повышение температуры кожи в месте воспаления, и, |
|
|
|
|
|
|
||
конечно, болевой синдром. Внутри везикул находится |
|
|
|
|
|
|
||
гной желтоватого цвета с большим количеством нейтрофилов.
У людей европеоидной и азиатской рас, количество нейтрофилов в каждом пуле примерно равно. У лиц негроидной расы, количество нейтрофилов в краевом пуле больше;
В кровеносных сосудах небольшого диаметра, циркулирующий пул нейтрофилов располагается в центральном осевом потоке;
Пул циркулирующих нейтрофилов можно оценить при проведении общего и клинического анализа крови с помощью гематологического анализатора или при мазках периферической крови;
Распределение нейтрофилов в этих пулах может быть изменено при активации/дезактивации молекул адгезии нейтрофилов (см. ниже).
5.2.Маргинация нейтрофилов
При ОВ, эритроциты агрегируют между собой, образуя «монетные столбики» в венулах. Это происходит благодаря фибриногену, образующемуся в печеночных клетках;
Появление «монетных столбиков» приводит к сдвигу нейтрофилов из центрального осевого потока на периферию. Этот процесс и называется маргинацией. Очень важно, отличать процесс маргинации нейтрофилов от краевого (маргинального) пула нейтрофилов;
5.3.Перекатывание нейтрофилов
Перекатывание нейтрофилов по эндотелиальной выстилке связано с появлением на клетках специальных молекул адгезии, н. селектина;
Селектины являются углевод-связывающими молекулами адгезии;
L-селектин располагается на лейкоцитах (н. на нейтрофилах), а E- и P-селектин на эндотелиальных клетках венул:
o Р-селектин продуцируется тельцами Уэйбеля-Палада в венулярных эндотелиоцитах;
o Тельца Уэйбеля-Палада являются «фактором склеивания» эндотелиоцитов, так как они продуцируют Р-селектин для адгезии лейкоцитов, и фактор Виллебранда для адгезии тромбоцитов.

Medicine Books (https://vk.com/medicinebook)
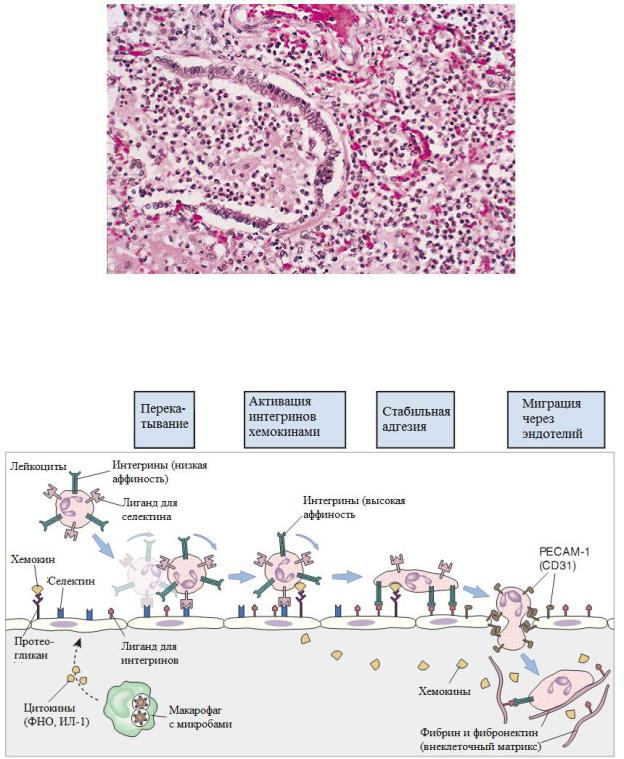
Рис 3-3: Перемещения нейтрофилов при остром воспалении. Перекатывание клетки по поверхности эндотелия активируется селектинами (адгезионные молекулы), которые плотно связываются с активированными β2-интегринами (CD11a:CD18) на поверхности нейтрофилов. После этого, нейтрофилы мигрируют сквозь базальную мембрану венул в окружающую ткань. При этом, в ткань выходят не только нейтрофилы, но и богатая белками плазма крови, образуя экссудат. Находящиеся в межклеточном пространстве хемоаттрактанты, направляют нейтрофилы в очаг воспаления.
Интерлейкин-1 (ИЛ-1) и фактор некроза опухоли (ФНО) стимулируют выработку лигандов для селектина на поверхности нейтрофилов и выброс селектиновых молекул на поверхности эндотелия венул – Е- и Р-селектинов (рис. 3-5);
Образующаяся связь между нейтрофилами с Е- и Р-селектинами на поверхности эндотелия венул слабая и непостоянная. Это приводит к постоянному перекатыванию нейтрофилов на поверхности клеток (циклы прилипанияотлипания, прилипания-отлипания и т.д.).
5.4.Экспрессия нейтрофилами β2-интегринов, обеспечивает их крепкую адгезию на эндотелиоцитах, имеюшихлиганды для интегринов.
Активация нейтрофильных β2-интегринов (CD11a:CD18)
oРасположенные на нейтрофилах β2-интегрины взаимодействуют с соответствующими лигандами на эндотелиоцитах венул (см. позже; рис. 3-
5);
o β2-интегрины активируются с помощью C5a и лейкотриенаB4 (LTB4);
oКатехоламины и кортикостероиды ингибируют процесс активации β2интегринов. Подобное ингибирование приводит к повышению количества нейтрофилов в периферической крови (нейтрофильный лейкоцитоз). Данное явление связано с откреплением нейтрофилов из краевого пула и их переходом в циркуляцию;
oЭндотоксины усиливают активацию β2-интегринов на нейтрофилах. Подобное явление приводит к снижению количества нейтрофилов в периферической крови (нейтропения), что связано с переходом клеток из циркулирующего пула в краевой.
Активация молекул адгезии (лигандов для интегрина) на эндотелиальных клетках
oИЛ-4 и ФНО активируют внутриклеточные молекулы адгезии (ICAM) и молекулы адгезии сосудистых клеток (VCAM) на эндотелии венул;
oАктивированные ICAM прикрепляются к активированным β2-интегринам на нейтрофилах, обуславливая их прочное прикрепление к венулярному эндотелию;
o АктивированныеVCAM связывают β1-интегрины на эозинофилах, моноцитах и лимфоцитах.
Заболевания, связанные с дефицитом адгезии лейкоцитов (ДАЛ) o Связанны с аутосомально-рецессивным насследованием;
Medicine Books (https://vk.com/medicinebook)
Рис 3-4: Острое воспаление. Гистологический препарат ткани легкого с бронхопневмонией. Видно большое количество нейтрофилов с сегментированными ядрами. Между клетками находится большое количество окрашиваемого в розовый цвет экссудата, богатого белками и клетками.
Рис 3-5: Последовательность событий при миграции лейкоцитов из крови в очаг инфекции. В очаге инфекции, макрофаги и дендритные клетки после контакта с бактериями, выделяют цитокины (н. фактор некроза опухоли (ФНО) и интерлейкин-1 (ИЛ-1)). Данные цитокины активируют эндотелиальные клетки рядом расположенных венул, стимулируя продукцию ими молекул селектинов, лигандов для интегринов, а так же ряда хемокинов. Селектины обеспечивают слабое взаимодействие эндотелиоцитов с нейтрофилов, и последние перекатываются по эндотелиальным клеткам. Интегрины обеспечивают плотный контакт между указанными клетками, а хемокины, в свою очередь, активируют нейтрофилы и стимулируют их миграцию через эндотелий в очаг инфекции. Моноциты крови и активированные Т-лимфоциты мигрируют в очаг инфекции по схожим механизмам. PECAM-1, platelet/endothelialcelladhesionmolecule 1.
Medicine Books (https://vk.com/medicinebook)
oДАЛ 1 типа возникает при дефиците β2-интегринов (CD11a:CD18). CD – кластер дифференцировки;
oДАЛ 2 типа возникает при дефиците селектинов на эндотелиальных клетках, которые в норме связывают нейтрофилы.
oКлинические признаки
Манифестация связана с задержкой отделения пуповины (в норме происходит в конце второй недели постнатального развития ребенка). Ферменты нейтрофилов играют важнейшую роль в этом процессе. При гистологическом исследовании, в сосудах и в интерстиции не наблюдается нейтрофилов;
Помимо этого, возникают частые гингивиты, отмечается замедленное заживление ран и нейтрофильный лейкоцитоз (отсутствие маргинального пула нейтрофилов).
5.5.Трансмиграция (диапедез) нейтрофилов
Нейтрофилы проходят между эндотелием венул и через базальную мембрану (выделяя коллагеназу IV типа) и входят в интерстициальную ткань;
Параллельно в интерстициальную ткань выходит плазма, богатая белками и клетками (экссудат, гной);
Функции экссудата:
oРазбавление бактериальных токсинов при их наличии;
oОбеспечение опсонизации (за счет IgG и C3b) для облегчения фагоцитоза (см. позже).
5.6.Хемотаксис нейтрофилов
Нейтрофилы двигаются по химическому градиенту хемоаттрактантов к месту локализации инфекционного процесса;
Медиаторы хемотаксиса (хемоаттрактанты) связываются с рецепторами на нейтрофилах – C5a, LTB4, бактериальные продукты и ИЛ-8;
Связывание приводит к высвобождению внутриклеточного кальция и повышению подвижности клеток.
5.7.Нейтрофильный фагоцитоз (рис. 3-6)
Нейтрофильный фагоцитоз – это многошаговый процесс, включающий в себя опсонизацию, поглощение и уничтожение.
Опсонизация
oОпсонины прикрепляются к бактерии или к инородному телу. К опсонинам относят IgG, C3bкомпонент комплемента и ряд других белков
(н. С-реактивный белок). Нейтрофилы имеют к данным молекулам рецепторы на своей поверхности;
oОпсонизация облегчает процесс узнавания нейтрофилами бактерий (и инородных тел) и прикрепление к ним;
oАгаммаглобулинемия Брутона – дефект процесса опсонизации (см. главу 4). При данном заболевании, пре-В клетки не созревают в В-клетки. В результате этого, плазматические клетки, происходящие из В-клеток, отсутствуют и иммуноглобулины (в частности IgG) не секретируются.
Поглощение
oНейтрофилы фагоцитируют бактерий, формируя фагоцитарную вакуоль (фагосому);
oПервичные лизосомы с гидролитическими ферментами сливаются с фагоцитарной вакуолью, образуя фаголизосому;
oПри синдроме Чидьяка-Хигаси (см. главу 2) наблюдается дефект в функционировании микротрубочек, что приводит к нарушению слияния лизосом с фагосомой и образованию фаголизосомы.
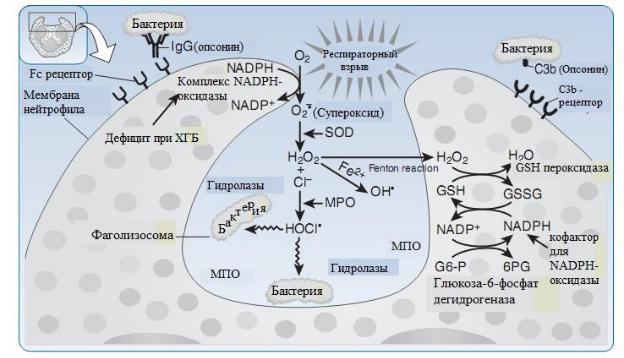
Уничтожение бактерий/грибков с помощью системы О2-зависимой миелопероксидазы (МПО) (см. рис. 3-6)
Medicine Books (https://vk.com/medicinebook)
Рис 3-6: Кислород-зависимаямиелопероксидазная система. В фаголизосомах происходит серия биохимических реакций, приводящая к продукции свободного радикала гиплохлорита (хлорка, HOCL.), который разрушает бактерий. Превращение H2O2 в гидроксильный радикал происходит при ипользованииFe2+в качестве источника электронов. Данная реакция носит названия «реакция Фентона». НАДФ-Н образуется с помощью пентозофосфатного шунта, и используется в качестве кофактора для НАДФ-оксидазы, недостаток который наблюдается при ХГБ. Снижение содержания кофакторов НАДФН (н. дефицит глюкоза-6-фосфат дегидрогеназы) приводит к нарушению нормального функционирования кислород-зависимоймиелопероксидазной системы. IgG и C3b являются опсонинами, облегчающими процесс фагоцитирования нейтрофилами и макрофагами.
ХГБ, хронические грануломатозные болезни;Fe2+, двухвалентное железо; GSH, редуцированный глутатион; G6-P, глюкоза-6-фосфат; GSSG, окисленный глутатион; H2O2, перекись водорода; МПО, миелопероксидаза; NADPH, окисленная форма никотинамидадениндинуклеотидфосфата; NADPH, восстановленная форма никотинамидадениндинуклеотидфосфата; OH-, гидроксильный анион; 6PG, 6- фосфоглюконат; SOD, супероксиддисмутаза.
o Система О2-зависимой МПО имеется только в нейтрофилах и моноцитах (отсутствует в макрофагах). МПО – нейтрофильный и моноцитарный лизосомальный фермент;
o Система МПО обладает высокой бактерицидной активностью;
oПродукция супероксидных свободных радикалов (СР):
НАДФ-Н оксидазный комплекс конвертирует молекулярный кислород в супероксидный СР. Данный процесс носит название
респираторного, или оксидативного взрыва.
oПродукция пероксида (H2O2):
Супероксиддисмутаза (СОД) превращает О2 в H2O2;
Определенная часть пероксида превращается в гидроксильный свободный радикал с помощью Fe посредством реакции Фентона (см. главу 2)
oПродукция «белизны» (HOCl.). МПО в фаголизосомах соединяет H2O2 с
ионом Cl, образуя гипохлорный СР (HOCl.), который уничтожает бактерии
и некоторые грибковые микроорганизмы.
oХроническая грануломатозная болезнь (ХГБ) и дефицит МПО, являются
примерами заболеваний, связанных с дефектом в системе О2-зависимой МПО.
Medicine Books (https://vk.com/medicinebook)
Хроническая грануломатозная болезнь (ХГБ) – может носить Х-сцепленный рецессивный характер наследования (65% случаев) или аутосомально-рецессивный характер (30% случаев). Х- сцепленные формы заболевания связанные с мутацией в гене CYBB, кодирующего важный компонент ферментного комплекса НАДФ-Н (система PHOX), что приводит к его дисфункции. Снижение продукции супероксидного радикала приводит к отсутствию респираторного (оксидативного) взрыва. Каталаза-положительные микроорганизмы могут продуцировать H2O2 (н.
Staphylococcusaureus, Nocardiaasteroids, Serratiamarcescens и грибы родов Aspergillus и Candida)
поглощаются, но не уничтожаются, в связи с воздействием каталазы на H2O2, продуцируемую
этими микроорганизмами. В то же время, свое функционирование продолжает МПО, но HOCl. не синтезируется из-за отсутствия H2O2. Однако, каталаза-негативные микроорганизмы (н. представители рода Streptococcus) поглощаются и могут быть уничтожены, так как МПО
комбинирует H2O2 с ионами Cl, образуя HOCl..
Грануломатозное воспаление происходит в тех тканях, где нейтрофилы фагоцитируют бактерии, но не могут уничтожить их. Подобные явления, главным образом, ассоциированы с хроническим воспалением и участием лимфоцитов с макрофагами. Макрофаги сливаются друг с другом, образуя многоядерные гигантские клетки, которые и являются характерной чертой грануломатозного воспаления. Пациенты с ХГБ имеют частые инфекционные заболевания, чаще всего связанные с грибковой микрофлорой и поражением легких (наиболее часто пневмонии), кожи, внутренних органов и костной системы. Классическим скрининг-тестом для ХГБ является тест с с нитросиним тетразолием (ТНБ). В этом тесте, лейкоциты помещаются в специальную пробирку и инкубируются с ТНБ, который приобретает синий цвет в случаи наличия супероксидных СР, что свидетельствует о наличии респираторного (оксидативного) стресса – это положительный тест. ТНБ тест отрицательный при Х-сцепленной форме ХГБ, так как ТНБ не конвертируется в синюю форму, что связан с дисфункцией комплекса оксидазных ферментов НАДФ-Н. Однако, подобный тест имеет низкую специфичность, поэтому замещается на окисление дигидрородамина до флюоресцирующего родамина, что наблюдается при всех вариантах ХГБ. Лечение ХГБ направлено на профилактику и лечение инфекций, и включает в себя трансплантацию костного мозга.
Дефицит миелопероксидозы (МПО) отличается от ХГБ тем, что наблюдается нормальный респираторный взрыв с образованием супероксидного радикала и Н2О2. Однако, нарушения в
работе МПО обуславливает нарушения синтеза HOCl..
oДефицит НАДФ-Н (н. недостаток глюкоза-6-фосфат дегидрогеназы (Г6ФД) приводит к дефектам в бактериоцидной активности:
НАДФ-Н кофакторНАДФ-Н оксидазного комплекса.
Пациенты с Г6ФД очень чувствительны к бактериальным и некоторым грибковым инфекциям, в связи с дисфункцией системы О2-зависимой МПО.
oУничтожение бактерий в нейтрофилах О2-независимой системой:
Кислород-независимые системы уничтожения бактерий связаны с выделением летальных субстанций, содержащихся в лейкоцитарнымх гранулах.
Гранулы содеражат: (а) Лактоферрин (содержится в гранулах нейтрофилов) связывает железо, которое необходимо для нормального бактериального роста и размножения; (б) Главный основной белок (ГОБ) находится в эозинофилах и обладает цитотоксичным действием на гельминтов.
6.Химические медиаторы при ОВ (Таблица 3-2):
6.1.Химические медиаторы находятся в плазме, лейкоцитах, в тканях организма и среди бактериальных производных. Например, медиаторы арахидоновой кислоты продуцируются из мембранных фосфолипидов в макрофагах, эндотелиальных клеток и тромбоцитов (рис. 3-7).
6.2.Они имеют короткий полупериод жизни (от нескольких секунд до минут).
6.3.Обладают местными и системными эффектами. Например, гистамин местно вызывает покраснение, а системно связан с анафилаксией.
Medicine Books (https://vk.com/medicinebook)
Таблица 3-1. Сравнение хронической грануломатозной болезни и дефицита миелопероксидазы
Заболевание |
Хроническая грануломатозная болезнь |
Дефицит миелопероксидазы |
Характер |
Х-сцепленный рецессивный |
Аутосомально-рецессивный |
наследования |
|
|
НАДФ-Н оксидаза |
Отсутствует |
Присутствует |
Миелопероксидаза |
Присутствует |
Отсутствует |
Респираторный |
Отсутствует |
Присутствует |
взрыв |
|
|
Пероксид (H2O2) |
Отсутствует |
Присутствует |
Хлорка (НОСl) |
Отсутствует |
Отсутствует |
Таблица 3-2. Источники и функции химических медиаторов
Медиатор |
Источник (ки) |
Функция (ии) |
Метаболиты арахидоновой кислоты |
|
|
Простагландины |
Макрофаги, эндотелиальные клетки, |
ПгЕ2: вазодилятация, боль, лихорадка |
|
тромбоциты |
ПгI2: вазодилятация, ингибирование |
|
ПгН2: главный предшественник Пг и |
агрегации тромбоцитов |
|
тромбоксанов |
|
Тромбоксан А2 |
Тромбоциты |
Вазоконстрикция, агрегация |
|
Образуется из ПгН2 с помощью |
тромбоцитов |
|
тромбоксансинтетазы |
|
Лейкотриены (ЛТ) |
Лейкоциты |
ЛТВ4: хемотаксис и активация |
|
|
нейтрофильных адгезионных молекул |
|
Образуются из арахидоновой кислоты с |
ЛТC4, ЛТD4, ЛТЕ4: вазоконстрикция, |
|
помощью липооксигеназа- |
повышение проницаемости венул, |
|
опосредованного гидроксилирования |
бронхоконстрикция |
|
|
Зилеутон ингибирует 5-липооксигеназу, |
|
|
что приводит к снижению синтеза ЛТВ4, |
|
|
ЛТC4, ЛТD4, ЛТЕ4 |
|
|
Монтелукаст антагонист |
|
|
лейкотриенновых рецепторов ЛТC4, |
|
|
ЛТD4, ЛТЕ4 |
Брадикин |
Продукт активации кининовой системы |
Вазодилятация, увеличение |
|
активированным фактором XII |
проницаемости венул, боль |
Хемокины |
Лейкоциты, эндотелиальные клетки |
Активация нейтрофилов и |
|
|
стимулирование их миграции через |
|
|
эндотелий к месту инфицирования |
|
|
(хемотаксис, см. рис 3-5) |
Комплемент |
Синтезируется в гепатоцитах (белки |
С3а, С5а (анафилотоксины): |
|
острой фазы) |
стимулируют выброс гистамина из |
|
|
тучных клеток |
|
|
С3b: опсонизация |
|
|
C5a: активация молекул адгезии |
|
|
нейтрофилов, хемотаксис |
|
|
С5-С9 (мембранно-атакующий |
|
|
комплекс): лизис клетки |
Цитокины |
|
|
ИЛ-1, ФНО |
Макрофаги (главный источник), |
Инициируют синтез в переднем |
|
моноциты, дендритные клетки, |
гипоталамусе ПгЕ2, что приводит к |
|
эндотелиальные клетки |
развитию лихорадки |
|
|
Активация молекул адгезии на |
|
|
эндотелиоцитах |
|
|
ФНО промотор апоптоза (см. главу 2) |
ИЛ-6 |
|
Первичный цитокин, увеличивающий |
|
|
Medicine Books (https://vk.com/medicinebook) |
|
|
|
|
|
синтез белков острой фазы (БОФ) в |
|
|
печени: ферритин, факторы коагуляции |
|
|
(н. фибриноген), и С-реактивный белок |
ИЛ-8 |
|
Хемотаксис |
Гистамин |
Тучные клетки (важнейший источник), |
Вазодилятация, увеличение |
|
тромбоциты, энтерохромаффиные клетки |
проницаемости венул |
Оксид азота (NO) |
Макрофаги, эндотелиальные клетки |
Вазодилятация, бактерицидное |
|
Свободные радикалы NOобразуются при |
воздействие |
|
превращении аргинина в цитрулин с |
|
|
помощью NO-синтетазы |
|
6.4.Медиаторы выполняют разные функции:
Расширение сосудов – гистамин, окись азота, ПгI2;
Сужение сосудов – тромбоксан А2 (ТКА2);
Повышение проницаемости венул – гистамин, брадикинин, ЛтC4, ЛтD4, ЛтE4, С3а и С5а (анафилатоксины);
Ощущение боли – ПгЕ2, брадикинин;
Повышение температуры тела - ПгЕ2, ИЛ-1, ФНО;
Хемотаксис – С5а, ЛтB4, ИЛ-8;
Активация синтеза в печени белков острой фазы (БОФ; фибриноген, ферритин, комплемент, гепсидин, С-реактивный белок) – ИЛ-6.
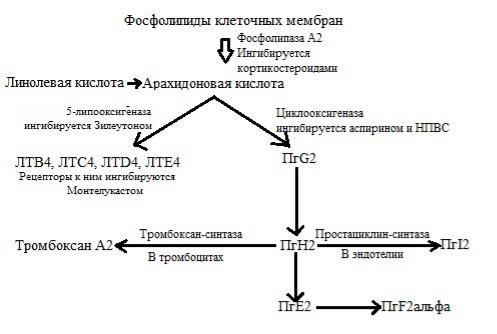
Рис 3-7: Метаболизм арахидоновой кислоты. Арахидоновая кислота получается из мембранных фосфолипидов с помощью фосфолипазы А2. В дальнейшем, она может превращаться в простагландины (Пг) или тромбоксанАав тромбоцитах из ПгН2, являющегося предшественником простагландинов, и в лейкотриены (ЛТ) посредством 5-липооксигеназы. Линолевая кислота, являющаяся ώ-6-ненасыщенной жирной кислотой может участвовать в синтезе арахидоновой кислоты. Фосфолипаза А2 ингибируется кортикостероидами; 5-липооксигеназа – Зилеутоном; рецепторы к ЛТС4, ЛТD4, ЛТЕ4 – Монтелукастом; а циклооксигеназа (ЦОГ) – аспирином и нестероидными противовоспалительными средствами (НПВС). ЦОГ- 1 экспрессируется во многих тканях, в то время как ЦОГ-2 индуцируется различными ростовыми факторами и провоспалительными цитокинами. См. текст и Таблицу 3-2 для более подробного описания.
НПВС – нестероидные противовоспалительные средства; ПгI2 – простациклин.
7.Типы острого воспаления
7.1.Локализация, причины и продолжительность воспаления определяют морфологическую картину воспалительной реакции.
Medicine Books (https://vk.com/medicinebook)
7.2.Гнойное воспаление:
Определение – локализованное воспаление, связанное с размножением гнойпродуцирующих микроорганизмов, таких как S.aureus (н. фурункулы на коже, рис.
3-8А);
S. aureus продуцирует коагулазу, которая расщепляет фибриноген до фибрина, тем самым удерживая бактерии и нейтрофилы в месте воспаления.
7.3.Фибринозное воспаление:
Определение – воспаление с увеличением проницаемости сосудов и отложением фибринового экссудата в тканях (рис. 3-8В).
Чаще всего наблюдается на серозных оболочках: перикард, брюшина или плевра: o При фибринозном перикардите, который может возникнуть в результате
инфаркта миокарда или острой ревматической лихорадки, может быть слышен шум трения листков перикарда (см. Главу 11).
o При фибринозном плеврите, связанном с пневмонией или инфарктом легкого, выслушивается шум трения плевры (см. Главу 17).
o Иногда, после проведения операций на органах брюшной полости, между органами образуются фиброзные спайки. В результате этого, возможно возникновение тонкокишечной непроходимости (см. Главу 18).
7.4.Серозное воспаление:
Определение – воспаление с большим количеством водянистого экссудата, в котором мало белковых молекул, в том числе и фибриногена.
Примеры – волдыри при ожогах второй степени, вирусные плевриты.
7.5.Псевдомембранозное воспаление:
Определение – повреждение слизистых оболочек в результате воздействия токсинов ряда бактерий, приводящее к появлению мембранозных образований, состоящих из некротизированной ткани.
Примеры:
o Псевдомембранозный колит, вызываемый Clostridium difficile (рис. 3-8С);
oОбразование псевдомембран в гортани и трахеи при инфицировании
Corynebacterium diphtheria (рис. 17-5D).
8.Роль лихорадки при остром воспалении:
8.1.Кривая связывания кислорода (КСК, см. главу 2) сдвигается вправо. Это приводит к увеличению доставки кислорода к тканям, что важно для системы О2-зависимой миелопероксидазы.
8.2.Повышение температуры неблагоприятно для бактерий и вирусов.
8.3.У госпитализированных пациентов лихорадка наиболее часто встречается при бактериальных инфекциях дыхательных путей, мочевыделительной системы, кожи и мягких тканей.
9.Ограничение длительности острого воспаления:
9.1.Все медиаторы ОВ имеют короткий период жизни.
9.2.Продукция липоксинов (противовоспалительные медиаторы):
Производные метаболитов арахидоновой кислоты (н. ЛКА4, ЛКВ4);
Ингибируют трансмиграцию и хемотаксис нейтрофилов;
Стимулируют поглощение апоптотических телец макрофагами.
