
- •Азотсодержащие соединения
- •Опыт 1. Образование и гидролиз сернокислой соли дифениламина (дфа)
- •Опыт 2. Цветная реакция дфа с hno3 и нитратами
- •Опыт 3. Щелочной гидролиз ацетамида
- •Опыт 4. Дезаминирование ацетамида
- •Опыт 5. Получение и свойства метиламина
- •Опыт 6. Взаимодействие первичных аминов с азотистой кислотой
- •Опыт 7. Растворимость мочевины в воде и образование ее азотнокислой соли
- •Опыт 8. Дезаминирование мочевины
- •Опыт 9. Гидролиз мочевины, доказательство ее строения
- •Опыт 10. Разложение мочевины при нагревании. Образование биурета и циануровой кислоты. Биуретовая реакция
- •Аминокислоты и белки
- •Опыт 1. Доказательство амфотерных свойств глицина
- •Опыт 2. Дезаминирование аминокислоты
- •Опыт 3. Образование медной соли глицина
- •Опыт 4. Биуретовая реакция – качественная на пептидную связь
- •Опыт 5. Качественные (цветные) реакции на боковые аминокислотные радикалы
ЛАБОРАТОРНАЯ РАБОТА № 9
Азотсодержащие соединения
Цель работы. Сопоставить свойства азотсодержащих соединений, познакомиться с их качественными реакциями.
Опыт 1. Образование и гидролиз сернокислой соли дифениламина (дфа)
На предметное стекло поместите несколько кристаллов ДФА, а на них 2-3 капли концентрированной H2SO4.
Стеклянной палочкой размешайте кристаллы до их растворения, т.е. до образования соли гидросульфата дифениламмония. С помощью стеклянной палочки перенесите часть раствора образовавшейся соли на другие участки предметного стекла (рис. 8) для проведения нескольких капельных проб на предметном стекле.
Д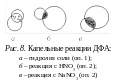 обавьте
на край одной из капель (другой палочкой)
каплю воды. В месте соприкосновения
раствора соли и воды немедленно происходит
гидролиз соли и выделение белого осадка
свободного ДФА. Напишите реакции
образования и гидролиза гидросульфата
дифениламмония.
обавьте
на край одной из капель (другой палочкой)
каплю воды. В месте соприкосновения
раствора соли и воды немедленно происходит
гидролиз соли и выделение белого осадка
свободного ДФА. Напишите реакции
образования и гидролиза гидросульфата
дифениламмония.
(Амины – органические основания. Анилин – (фениламин) –более слабое основание, чем алифатические амины: неподеленная пара электронов азота взаимодействует с сопряженной электронной системой бензольного ядра. Введение второй фенильной группы еще больше ослабляет основные свойства аммиака, ДФА образует соли только с концентрированными кислотами, а при разбавлении водой немедленно происходит гидролиз соли).
Опыт 2. Цветная реакция дфа с hno3 и нитратами
Приготовьте очень разбавленный раствор азотной кислоты: в боль-шой пробирке к капле конценрированной HNO3 долейте воды почти до верха.
Одну каплю полученного разбавленного раствора HNO3 поместите на предметное стекло рядом с каплей сернокислого раствора ДФА. В мес-те соприкосновения капель (см. рис. 7, б) появляется интенсивное синее окрашивание.
Чтобы избежать гидролиза при проведении цветной реакции, нуж-но остерегаться избытка воды.
Дифениламин является реактивом на HNO3, так как при действии ее на раствор ДФА в конц. H2SO4 образуется темно-синего цвета аммониевая соль дифенилбензидина:
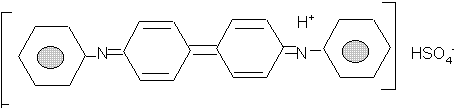
Интенсивная окраска вещества обусловлена наличием в молекуле системы сопряженных двойных связей.
Реакция используется для количественного колориметрического определения концентрации HNO3.
Сделайте аналогичные пробы с растворами NaNO3, NaNO2, KMnO4. Эта реакция очень чувствительна и широко используется для санитарно-химического контроля загрязнения овощей нитратами, а рек – сточными водами.
Опыт 3. Щелочной гидролиз ацетамида
Несколько кристаллов ацетамида поместите в пробирку, добавьте 10 капель 2н. NaOH и нагрейте. Резкий запах аммиака и посинение лакмусовой бумаги свидетельствует о гидролизе ацетамида.
Напишите уравнения реакций.
Опыт 4. Дезаминирование ацетамида
Поместите в пробирку несколько кристаллов ацетамида, добавьте 8 капель 10 %-го раствора NaNO2 и 2 капли концентрированной HNO3. Нагрейте на спиртовке.. Влажным красным лакмусом обнаружьте аммиак.
Напишите уравнение реакции дезаминирования ацетамида.
Опыт 5. Получение и свойства метиламина
Предварительно приготовьте три пробирки с испытательными растворами:
(а) в первую пробирку налейте 1 мл дистиллированной воды, в две другие пробирки – по 2 мл:
(б) 3 %-го раствора FeCl3 и
(в) 3 %-го раствора CuSO4.
В сухую пробирку внесите 0,5-1 г хлорида метиламмония и 1–2 г натронной извести. Смесь тщательно перемешайте стеклянной палочкой. Пробирку закройте пробкой с газоотводной трубкой и закрепите в лапке штатива. Реакционную смесь нагрейте на спиртовке:
[CH3 – NH3]+Cl– + NaOH = CH3 – NH2 + NaCl + H2O.
К отверстию газоотводной трубки, из которой выделяется газообразный метиламин, поднесите стеклянную палочку, смоченную концентрированной HCl – палочка окутывается туманом:
CH3 – NH2 + HCl = [CH3 –NH3]+Cl–
Через испытательные растворы пропустите газообразный метиламин.
Испытайте реакцию среды в пробирке (а) – водный раствор амина.
В пробирке (б) с FeCl3 через некоторое время выпадает бурый осадок
СН3 – NH2 + H2O = [CH3 –NH3]+OH–
3 [CH3 –NH3]+OH– + FeCl3 = Fe(OH)3 + 3 [CH3 –NH3]+Cl–
В пробирке (в) с CuSO4 вначале образуется голубой осадок Cu(OH)2, который растворяется в избытке метиламина. Запишите соответствующие уравнения реакций.
