
296_p1828_C14_9232
.pdfМинистерство образования и науки Российской Федерации
ГОУ ВПО Иркутский государственный университет Химический факультет
ОРГАНИЧЕСКАЯ ХИМИЯ
Часть 2 КОВАЛЕНТНАЯ ХИМИЧЕСКАЯ СВЯЗЬ
Методические указания

2
Печатается по решению ученого совета химического факультета Иркутского государственного университета
Рецензент проф. Б. В. Тимохин
Составители:
доц. Б. Л. Финкельштейн, проф. В. Н. Кижняев доц. А. Г. Пройдаков, доц. Е. Ф. Рохина доц. Г. Г. Шевченко, доц. О. А. Эдельштейн
Рассмотрены основные положения современной теории ковалентной (локализованной и делокализованной) химической связи, основанные на методе МО ЛКАО (молекулярные орбитали – линейная комбинация атомных орбиталей). Введены понятия индукционного эффекта – для локализованных σ-связей и мезомерного эффекта – для делокализованных π-связей как методов оценки распределения электронной плотности на качественном уровне. Кратко охарактеризованы спектральные характеристики ковалентных связей. Для закрепления материала составлены упражнения и свод основных определений по темам.
Все изложенные материалы соответствуют стандарту бакалавра химии, отражают современные достижения органической химии, имеют практикоориентированную направленность. Способствуют формированию у студентов учебных компетенций, необходимых в профессиях химического направления.
Предназначены для студентов 2-го курса химического факультета.
Библиогр. 7 назв. Ил. 18. Табл. 3
3
ОГЛАВЛЕНИЕ
Введение ................................................................................................................
Атомные орбитали (АО) ...................................................................................
Молекулярные орбитали (МО) .......................................................................
Локализованная ковалентная связь ..............................................................
Длина и энергия связи .................................................................................
Гибридизация ..............................................................................................
Электроотрицательность .......................................................................
Индуктивный эффект и эффект поля ....................................................
Делокализованная химическая связь ............................................................
Делокализованные связи в насыщенных молекулах ................................
Делокализованные π-орбитали. Сопряжение .........................................
Метод резонансных структур .................................................................
Полярные сопряженные молекулы. Мезомерный эффект ....................
σπ–Сопряжение. Гиперконьюгация (сверхсопряжение) ........................
Спектральные характеристики органических молекул.............................
Фотоэлектронная спектроскопия и электронная.
трансмиссионная спектроскопия ...........................................................
УФ-спектроскопия и спектроскопия в видимой области .....................
ИК-спектроскопия. Колебательные спектры.........................................
Радиоспектроскопия ядерного магнитного резонанса (ЯМР) .............
Упражнения ...........................................................................................................
Рекомендуемая литература ..................................................................................
4

Введение
Общепринятый в настоящее время способ изображения структурных формул органических молекул базируется на электронной теории химической связи, разработанной Дж. Льюисом.
Ковалентная химическая связь – результат спаривания двух электронов с противоположными спинами, принадлежащих атомам, образующим связь (ковалентная связь есть «поделенная» электронная пара).
Выигрыш в энергии – за счет спаривания электронов.
В структурных формулах поделенная электронная пара обозначается черточкой.
Современная теория химической связи рассматривает атомы и молекулы, как квантово-механические системы, подчиняющиеся уравнению Шредингера. Вся информация о динамических свойствах электрона содержится в соответствующей ему волновой функции. Электронам, находящимся в поле одного (или нескольких) атомных ядер, соответствуют атомные (или молекулярные) волновые функции.
Волновая функция является решением уравнения Шредингера, описывающего состояние электрона в атоме или молекуле:
HΨ = ЕΨ,
Е– собственные («разрешенные») значения энергии системы (Е1, Е2, Е3, ..., Еn).
Ψ– волновые функции Ψ1,Ψ2,Ψ3,...Ψn, соответствующие Е1, Е2, Е3, …, Еn.
Н – оператор Гамильтона полной энергии системы
Н = –ћ 2/2me (д2Ψ/дx2+ д2Ψ/дy2 + д2Ψ/дx2) + V(x, y, z)Ψ,
где me и V – приведенная масса электрона и его потенциальная энергия в поле ядра или нескольких ядер).
Атомные орбитали (АО)
Электрон в поле атомного ядра является квантово-механической системой и может обладать только определенными, дискретными («разрешенными»,
т. е. являющимися решениями уравнения Шредингера) значениями энергии Еi. Поскольку для такой системы справедлив принцип неопределенности Гейзенберга (невозможно одновременно и точно измерить координаты и энергию электрона), исчезает понятие точной траектории или орбиты в окрестностях атомного ядра, по которой движется электрон, имеющий данное значение энер-
5
гии Еi. Можно говорить лишь о большей или меньшей вероятности его обнаружения в данной точке вблизи или вдали от трехмерной поверхности максимальной электронной плотности (сферической или более сложной формы). Электрон, а следовательно, и его электрический заряд, как бы размывается в трехмерное «электронное облако» вблизи этой поверхности. Возникает понятие
орбиталь.
Еi – разрешенное значение энергии для данной атомной орбитали (одно
из собственных значений оператора Гамильона), а φi – волновая вероятностная функция. Квадрат этой функции указывает на вероятность обнаружения электрона, обладающего энергией Еi в точке с координатами (х, y, z), что эквивалентно плотности отрицательного заряда (в единицах заряда электрона) в точке (x, y, z) электронного облака атомной орбитали (АО) с данным разрешенным значением энергии Еi:
ϕ2(x, y, z) = ρ (x, y, z).
Численное значение самой волновой функции есть значение амплитуды вероятности обнаружения электрона в этой точке. Понятие амплитуды возникает из периодичности функции, поэтому ее называют волновой.
Атомная волновая функция должна быть непрерывна, дифференцируема (требования гамильтониана) и нормирована (по физическому смыслу), так как суммарная вероятность обнаружения электрона по всему пространству должна
быть исчерпывающей (равной единице), т. е.
–∞ ∫ ∞φ2dτ = 1.
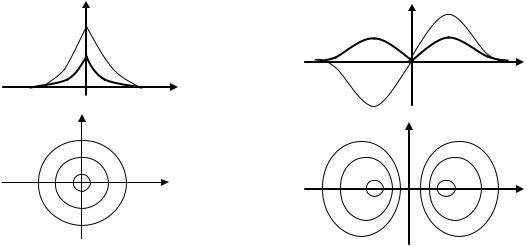
Функции распределения электронной плотности можно изобразить в виде
графиков, сечений или граничных поверхностей. Графики волновых функций
и их квадратов вдоль оси х и контуры (сечения) ϕ в плоскости хy для 1s- и 2рx- орбиталей водорода (ядро находится в начале координат) приведены на рис. 1.
|
z |
|
z ϕ |
|
|
ϕ |
|
ϕ2 |
ϕ2 |
|
|
ϕ2 |
х |
|
|
х |
|
|
ϕ |
|
|
||
y |
1s-орбиталь |
2px – орбиталь |
|||
|
|||||
|
у |
|
|||
0,1 |
|
- 0,2 |
0,2 |
||
|
|
||||
0,2 |
|
- 0,3 |
0,3 |
|
|
0,4 |
x |
- 0,4 |
0,4 |
х |
|
|
|||||
Рис. 1. Графики и сечения 1s- и 2px-орбиталей атома водорода
6

n |
1 |
|
|
|
2 |
|
|
|
Z |
|
X |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
l |
|
|
|
|
|
|
|
|
Y |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
0 |
|
|
1 |
|
|
0 |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
ml |
0 |
0 |
– 1 |
0 |
+ 1 |
0 |
–1 |
0 |
+1 |
–2 |
–1 |
|
0 |
+1 |
|
+2 |
||||||||
Сечение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
а) радиаль- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ных узл. |
н один нет |
нет |
нет |
два |
один |
один один |
нет |
нет |
|
нет |
нет |
|
нет |
|||||||||||
б) угловых е |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
узлов |
т нет один один один |
нет |
один |
один один |
два |
два |
|
два |
два |
два |
||||||||||||||
Граничн. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
поверх- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ность |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
2 |
Cимвол |
1s |
2s |
2p |
x |
2p |
2p |
z |
3s |
3p |
x |
3p |
y |
3p |
z |
3d |
xy |
3d |
3d |
3d |
yz |
d |
|||
|
|
|
|
y |
|
|
|
|
|
|
|
x – y |
xz |
|
z |
|||||||||
|
|
|
2s-орбиталь; |
|
3р-орбиталь; |
|
|
3d-орбиталь |
|
|
|
|
|
|
||||||||||
|
|
вложенные сферы |
вложенные гантели |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
Радиальные узлы |
|
|
Угловые |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
(узловые поверхности) |
узлы |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
Рис. 2. Сечения и граничные поверхности s-, p- и d-орбиталей |
|
|
|
|
|
|||||||||||||||||
Функция ϕ(1s) симметрична относительно начала координат, а функция ϕ(2рx) антисимметрична, так как знак амплитуды меняется при переходе через начало координат вдоль оси х (функция имеет узел). При этом значения электронной плотности ϕ2(2рx) в точках (x,z) и (-x,z) одинаковы.
Граничные
поверхности s- и р-
орбиталей
Граничная поверхность (трехмерное изображение) s-орби- тали – сфера, ограничивающая объем вокруг ядра, в котором вероятность обнаружения электрона близка к единице. Объемное изображение р-орбитали – «гантель». Поскольку необходимо учитывать знак амплитуды р-функ- ции, одну лопасть (отрицательную) выделяют цветом.
Атомная орбиталь (АО) и волновая функция характеризуются тремя квантовыми числами: главным (n), орбитальным (l) и магнитным (ml). Главное квантовое число n указывает номер оболочки и задает количество радиальных узлов (узловых поверхностей, на которой волновая функция меняет знак). Орбитальное квантовое число l задает количество угловых узлов (секторов, в которых волновая функция имеет различный знак амплитуды вероятности); l мо-
7

жет принимать значения от 0 до n – 1. АО с l = 0, 1, 2 и 3 называют соответственно s-орбиталями, р-орбиталями, d-орбиталями и f-орбиталями. Магнитное
кван-товое число ml задает ориентацию АО относительно ядерных координат. Квантовое число ml изменяется в интервале от –l через нуль до +l. Из этого следует существование трех р-орбиталей c одинаковой энергией. Такие орбитали называются вырожденными. Таким образом, р-орбиталь трехкратно вырождена, а d- и f-орбитали вырождены соответственно пяти- и семикратно (рис. 2).
Важнейшими характеристиками орбитали являются: энергия (определяется главным и орбитальным квантовыми числами n и l), симметрия (задается
квантовым числом l ) и ориентация относительно ядерных координат (ml ). Собственные значения энергии Еi для АО располагаются в следующем
порядке (по мере возрастания):
1s < 2s < 2p < 3s < 3p < 4s ≈ 3d < 4d < 4p < 5s ≈ 4d < 5p < 5d ≈ 4f
Из приведенного ряда следует, что чем больше узлов имеет волновая функция, тем выше энергия соответствующей АО.
Квадрат атомной волновой функции описывает распределение электронной плотности в окрестностях атомного ядра при данном разрешенном значении энергии электрона.
АО характеризуется энергией, симметрией и ориентацией относительно атомного ядра.
АО, имеющие одинаковую энергию, называются вырожденными.
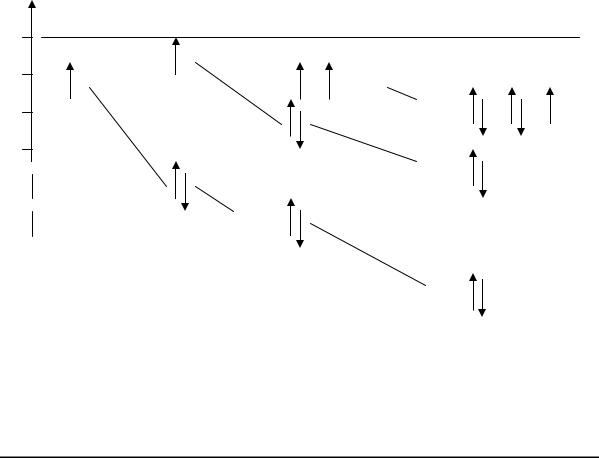
Атомная орбиталь может быть свободной, занятой одним неспаренным электроном или дважды занятой электронами с противоположными значениями спинового квантового числа s = ±1/2 в соответствии с принципом Паули. Энергия занятых АО определяет их потенциал ионизации (ПИ), энергия свободных орбиталей определяет их сродство к электрону (СЭ). Ниже приведены диаграммы заполнения АО и их энергии (потенциалы ионизации) для основных состояний атомов водорода, лития, углерода и фтора (рис. 3).
Энергии одноименных орбиталей снижаются с увеличением заряда ядра. Особенно сильно этот эффект выражен для внутренних слоев электронов. Высокие потенциалы ионизации внутренних электронов препятствуют их участию в образовании химической связи. Поэтому валентными называют только электроны внешних (незаполненных) уровней.
8
0
–10
–20
–30
– 70
–300
–700
|
|
5.4 eV |
|
2s уровень свободных электронов |
|
|
|
|
|
|
||||||
|
|
1s |
|
11.3 eV |
|
|
|
|
|
2p |
|
|
|
|
2p |
|
13.6 eV |
|
24.4 eV |
|
|
|
|
|
17.4 eV |
|
|
|
|
||||
|
|
2s |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
Н
≈ |
75.6 eV |
|
1s |
37.8 eV |
2s |
|||
|
|
|
|
|
|
|||
≈ |
|
|
288 eV |
1s |
|
|||
|
|
|
|
|
||||
|
|
|
Li |
|
|
|
|
|
≈ |
|
C |
|
|
F |
|||
|
|
|
|
|
||||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
694 eV |
1s |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 3. Энергия и заполнение АО в атомах водорода (Н), лития (Li), углерода (С) и фтора (F)
Молекулярные орбитали (МО)
Молекула является более сложной квантово-механической системой, чем атом. Электроны находятся в поле нескольких атомных ядер. Решение уравнения Шредингера для такой системы представляет очень сложную математическую задачу – необходимо решить уравнение Шредингера для каждого электрона, находящегося одновременно в поле всех ядер и других электронов, входящих в молекулу. Одним из эффективных и физически обоснованных приближений для решения этой задачи является метод, в котором для построения
волновых функций электронов в молекуле (Ψj) используется линейная комбинация относительно более простых атомных волновых функций φi (метод МО ЛКАО). Как правило, учитываются только валентные электроны атомов.
Ψj = Σcij φi ,
где коэффициент сij отражает вклад i-й АОφi в j-ю МО Ψj.
Молекулярные волновые функции Ψj должны удовлетворять тем же требованиям, что и атомные: быть непрерывными и дифференцируемыми (эти требования выполняются автоматически, так как линейная комбинация φi не нарушает этих условий) и нормированными, т. е. интеграл по всему пространству для Ψ2 должен равняться единице:
-∞ ∫ ∞Ψ 2dτ = 1
Последнее условие выполняется, если сумма квадратов всех коэффициентов с которыми все i-е АО участвуют в одной j-й МО будет равна единице
9

∑сij2 = 1 (суммирование по i-м АО для любой j-й МО), i
но тогда сумма квадратов коэффициентов, с которыми каждая данная АО φi
участвует во всех полученных МО Ψj (и связывающих и разрыхляющих) также должна равняться единице.
∑сij2 = 1, (суммирование по j-м МО для любой i-й АО) j
Одновременное выполнение условий для коэффициентов МО ЛКАО
∑сij2 = 1 |
∑сij2 = 1 |
j |
i |
позволяет обнаружить с вероятностью, равной единице, все электроны, принадлежавшие ранее атомам (и находившиеся на атомных орбиталях φi) в образовавшейся из этих атомов молекуле (на молекулярных орбиталях Ψj).
Рассмотрим, как можно скомбинировать две s-АО атомов водорода для построения МО молекулы Н2 (рис. 4.). В простейшем случае, когда взаимодействуют два одноэлектронных атома, существуют только две линейные комбинации их АО: сумма и разность.
Е |
|
Ψ2* = c21φ1 – c22φ2 |
перекрывание в противофазе |
|
(амплитуды вычитаются) |
||
|
|
c21 = c22 |
|
–∆Е |
φ1(1s) |
φ2(1s) |
|
|
|
Ψ1 = c11φ1+ c12φ2 |
|
|
|
c11 = c12 |
перекрывание в фазе |
|
|
|
|
|
|
|
(амплитуды суммируются) |
Рис. 4. Метод МО ЛКАО для молекулы водорода
Комбинация Ψ1, когда перекрываются атомные волновые функции с одинаковым знаком амплитуды вероятности (в фазе), сопровождается понижением энергии, т.к. суммарная амплитуда вероятности обнаружения электронов в об-
ласти между ядрами увеличивается, а перекрывание в противофазе (Ψ2* – раз-
ностная функция) сопровождается повышением энергии, так как Ψ2* имеет узел в межъядерной области (рис. 4). Очевидно, что оба имеющихся электрона в невозбужденной молекуле в соответствии с принципом Паули могут занять орбиталь Ψ1, при этом имеется выигрыш в энергии (–2∆Е) и может образоваться связь, поэтому МО Ψ1 называется связывающей. Если будет заселяться МО
Ψ2*, энергия системы повышается, и эту орбиталь называют разрыхляющей
10
